В настоящее время эндопротезирование коленного сустава является одним из самых востребованных и высокоэффективных методов лечения многих заболеваний и последствий травматических повреждений коленного сустава, в частности остеоартроза. В Российской Федерации заболеваемость остеоартрозом составляет в среднем 18 человек на 10000 населения [1]. Наибольшая потребность в этом виде хирургического лечения в последние годы возникает среди пациентов моложе 65 лет, притом, что в 2005 году возрастной ценз находился в пределах от 65 до 74 лет. Это связано с прогрессивным ростом населения Земли, числа людей, страдающих от наличия избыточной массы тела, а также увеличением доли людей с потребностью вести активный образ жизни, несмотря на возраст и наличие заболеваний опорно-двигательного аппарата [2]. С увеличение оперативных вмешательств по поводу эндопротезирования коленного сустава растет и количество ревизий, связанных как с инфекцией области хирургического вмешательства, так и с нестабильностью компонентов эндопротеза. Очень часто после таких операций встает вопрос о замещении костного дефеката с целью дальнейшего реэндопротезирования, либо формирование артродеза коленного сустава индивидуальной конструкцией, в случае, если по какой-либо причине невозможно реэндопротезирование.
Факторы риска, определяющие выполнение реэндопротезирование коленного сустава.
В первое десятилетие после первичного тотального эндопротезирования коленного сустава (ТЭКС) наблюдаются отличные и хорошие результаты более чем в 92% случаев [3]. Результаты анализа статистических данных регистра эндопротезирования коленного сустава Новосибирского НИИТО им. Я.Л. Цивьяна за период с 2010 по 2015 г. показывает, что на долю реэндопротезирования коленного сустава приходится около 8% от общего объема выполненных ТЭКС [4]. Выделяют ряд наиболее частных причины выполнения реэндопротезирования: 23,1% приходится на асептическую нестабильность компонентов эндопротеза; 18,4% ревизий производится из-за возникновения инфекционных осложнений; 18,1% – из-за износа полиэтиленового вкладыша; 17,7% – в связи с несостоятельностью капсульно-связочного аппарата; в 9,3% случаев пациентов беспокоили постоянные боли и неудовлетворительный объем движений в оперированном суставе; в 4,5% случаев ревизионное вмешательство выполнено по поводу остеолиза вокруг компонентов эндопротеза; в 2,9% – диагностирована травматическая диспозиция компонентов эндопротеза [7].
Принципиально стоит выделить две категории пациентов требующих реэндопротезирования коленного сустава: первая – имеющие инфекционные осложнения и вторая – с отсутствием таковых. Данный фактор имеет определяющее значение в выборе тактики и объема последующего оперативного вмешательства.
При асептических осложнениях первоочередной задачей для хирурга является – восстановление механической части компонентов эндопротеза: одноэтапное реэндопротезирование ревизионным конструкциями с достижением надежной фиксации и трибологических свойств эндопротеза и связочной стабильности.
Однако если речь идет о возникновении перипротезной инфекции первостепенной является задача эффективной эрадикации инфекции, снижение болевого синдрома, максимально возможное сохранение объема движений коленного сустава.
Bono J.V. с соавторами предлагает следующие варианты хирургической тактики лечения перипротезной инфекции [8]:
Открытый дебридмент с заменой полиэтиленового вкладыша и сохранением компонентов эндопротеза.
Тактика, подразумевающая удаление компонентов эндопротеза: одноэтапная реимплантация; двухэтапная реимплантация с формированием спейсера.
Альтернативные виды хирургических вмешательств:
резекционная артропластика;
артродез выполняется с применением аппарата внешней фиксации, интрамедуллярного штифта, индивидуальной конструкции.
Как в случаях асептической, так и инфекционной нестабильности формируются обширные дефекты кости, не позволяющие в последующем выполнить реэндопротезирование сустава стандартными конструкциями, в связи с невозможностью достичь должной стабильности. Именно в этих случаях встает вопрос о выполнении артродеза коленного сустава.
Достоинства и недостатки выполнения артродезирования коленного сустава.
Выполнение артродеза позволяет эффективно бороться с инфекционными осложнениями, стабилизирует коленный сустав во фронтальной и сагиттальной плоскости, купирует болевой синдром, сохраняет опороспособность нижней конечности. Но все эти преимущества нивелируются невозможностью артикуляции в коленном суставе, что делает весьма затруднительным пребывание пациента в положении сидя, а также многие другие аспекты повседневной жизни [5].
Артродез является операцией выбора при наличии массивного дефекта костной ткани бедренной и большеберцовой костей, не позволяющего установить ревизионную конструкцию. Несостоятельность или отсутствие разгибательного аппарата, многократные рецидивы инфекции, а также наличие полирезистентных микроорганизмов или микробных ассоциаций, трудно поддающихся антибактериальной терапии, также являются показаниями к проведению артродеза коленного сустава.
Существует несколько методик артродезирования коленного сустава при наличии инфекции: наложение аппарата внешней фиксации (АВФ), либо при помощи блокируемого стержня. В случае отсутствия инфекции: при помощи интрамедуллярного стержня, индивидуальной двухкомпонентной конструкцией с функцией артродеза. В виду доступности, относительной безопасности и технической простоты исполнения, наибольшее распространение получил аппарат внешней фиксации и артродез коленного сустава при помощи блокируемого стержня. Однако, как и все вышеописанные подходы к лечению хронической глубокой инфекции области оперативного вмешательства, использование АВФ может сопровождаться рядом осложнений: повреждение сосудисто-нервного пучка, воспалительные процессы мягких тканей и переломы в местах проведения спиц и стержней. Формирование артродеза блокируемыми интрамедуллярными стержнями нередко осложняется переломом или миграцией стержня, не исключен и рецидив инфекции (от 41 до 53%) за счет недостаточной стабильности конструкции [9].
Цель исследования
Рассмотреть возможность использования индивидуальных артродезирующих конструкций в ревизионном эндопротезирование коленного сустава с учетом определения плотности костной ткани по шкале Хаунсфилда. Привести методологию создания индивидуальных объемных конструкций с использование виртуального моделирования и технологий объемной печати.
Материалы и методы
Производство индивидуальных конструкций с функцией артродеза коленного сустава с использованием аддитивных технологий подразумевает несколько этапов. Связано это с тем, что каждое изделие будет обладать исключительными характеристиками, учитывающими особенности анатомии и форму дефекта бедренной и большеберцовой кости.
На первом этапе проводится МСКТ (спиральное сканирование, с толщиной слоя 0,5 мм, 2,0±0,9 мЗв) (рис.1). Полученные данные в виде серии DICOM-файлов с использованием специализированного программного обеспечения конвертируются в 3D-модель дефекта в формате obj [11]. Таким образом, появляется возможность работать с 3D моделью необходимой области опорно-двигательного аппарата (рис. 2).
Рис.1.МСКТ области коленного сустава
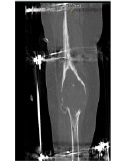
Рис. 2. Объемная модель дефекта (внешний вид, масштаб 1:3,5)

Данный формат совместим с программами 3D-обработки визуальных объектов (Autodesk 3D Studio Max, Autodesk Maya и др.) [12]. Эти программы обладают расширенными возможностями объемного моделирования и виртуального скульптинга.
Далее стандартными средствами программного обеспечения выполняется моделирование компонентов артродезирующей конструкции с учетом индивидуальных особенностей дефекта бедренной и большеберцовой костей, а также с учетом плотности костной ткани (рис. 3). Для количественной оценки плотности, визуализируемых методом МСКТ костных структур, используется шкала ослабления рентгеновского излучения, получившая название шкалы Хаунсфилда. Диапазон единиц шкалы («денситометрических показателей»), соответствующих степени ослабления рентгеновского излучения анатомическими структурами организма, составляет от -1024 до +3071, т.е. 4096 чисел ослабления. Средний показатель в шкале Хаунсфилда (0 HU) соответствует плотности воды, отрицательные величины шкалы соответствуют воздуху и жировой ткани, положительные – мягким тканям, костной ткани и более плотному веществу.
Рис. 3. Артродезирующая конструкция (внешний вид, масштаб 1:3,5)

В каждом клиническом случае измеренные показатели ослабления могут несколько отличаться на разных аппаратах, но на практике этим можно пренебречь. При оценке сложной анатомо-гистологической структуры измерение её «рентгеновской плотности» не всегда даёт возможность с точностью утверждать, какая ткань визуализируется, именно для этого проводится виртуальная объемная реконструкция результатов МСКТ, в ходе которой удаляются «шумы» и мягкие ткани.
Результаты
На полученной виртуальной модели проводится адаптация мест прилегания имплантата к области деформации и, при необходимости, модификация его формы и коррекция конгруэнтности компонентов имплантата и костных поверхностей (рис. 4). После завершения 3D-моделирования имплантата его модель сохраняется в формате stl, необходимом для CAD/CAM-производства, файл имплантата изготавливается на 3D принтере методом SLS печати (селективное лазерное спекание). Технология выборочного лазерного спекания (SLS) подразумевает использование одной или нескольких лазерных установок (как правило, углекислотных) для спекания частиц порошкообразного материала до образования заданного объекта. В качестве расходных материалов используются пластики, металл, керамика или стекло. Спекание производится за счет вычерчивания контуров, заложенных в цифровой модели с помощью направленного лазерного луча. По завершении спекания очередного слоя, рабочая платформа опускается, и наносится новый слой материала. Процесс повторяется до образования объемной модели, при этом в отличие от таких методов аддитивного производства, как стереолитография (SLA) или метод послойного наплавления (FDM), при SLS печати навесные части модели поддерживаются неизрасходованным материалом. Такой подход позволяет добиться практически неограниченной геометрической сложности изготовляемых моделей. Данный метод печати допускает использование EMI титана, разрешенного к имплантации системой сертификации ISO, именно его используют нейрохирурги при замещении дефектов костей черепа [13,14].
Рис. 4. Внешний вид замещения дефекта (масштаб 1:3,5)

Предложенная технология позволяет заместить дефекты кости любого объема, обеспечив стабильность и опороспособность коленного сустав, при этом сокращая сроки реабилитации пациента.
Заключение
В ходе работы было выполнено индивидуальное объемное моделирование бедренного и тибиального компонентов имплантата с возможностью формирования артродеза. С помощью возможностей специализированного программного обеспечения соблюдена высокая степень конгруэнтности костных структур и компонентов конструкции, данная процедура выполнена с учетом плотности костной ткани оцениваемой по шкале Хаунсфилда. Данная конструкция имеет ряд преимуществ: устанавливается одномоментно, подразумевает раннюю активизацию пациента, относительно просто демонтируется в случае возможной установки компонентов эндопротеза, наибольшая стабильность и механическая надежность конструкции в сравнении с используемыми методами.
Библиографическая ссылка
Баитов В.С., Мамуладзе Т.З., Базлов В.А. ВОЗМОЖНОСТИ ИСПОЛЬЗОВАНИЯ ОБЪЕМНОГО МОДЕЛИРОВАНИЯ И 3D ПЕЧАТИ С ЦЕЛЬЮ СОЗДАНИЯ ИНДИВИДУАЛЬНЫХ АРТРОДЕЗИРУЮЩИХ КОНСТРУКЦИЙ В РЕВИЗИОННОМ ЭНДОПРОТЕЗИРОВАНИИ КОЛЕННОГО СУСТАВА // Международный журнал прикладных и фундаментальных исследований. – 2016. – № 12-7. – С. 1189-1193;URL: https://applied-research.ru/ru/article/view?id=11010 (дата обращения: 20.04.2024).

