Некоторые тройные халькогениды молибдена получены методом синтеза и установлено, что при низкой температуре они обладают крайне высокой проводимостью [3]. Тиомолибдаты тяжелых металлов мало изучены. В литературе очень редко встречаются сведения о получении тиомолибдатов цинка, аммония серебра тиомолибдата. Например, в работе [4] имеются сведения об использовании тиомолибдата цинка как фотокаталитического катализатора при разложении воды. В работе [5] проведен синтез аммония серебра тиомолибдата из тиомолибдата аммония и азотнокислого серебра при условии стехиометрии. Полученное соединение черного цвета термически неустойчиво. Аналог этого соединения – аммоний, медь, тиомолибдат кристаллизуется в тетрагональной форме и используется как селективный катализатор при конверсии газов для получения этанола и высокоатомных спиртов.
Настоящее изобретение [6] описывает синтез новых тиомолибдатов; четыре конкретные соединения являются тио- и дитиомолибдатами серебра. Способ приготовления: реакции ионного соединения обладают хорошими трибологическими свойствами, при комнатной температуре до 500°С могут быть использованы в качестве твердой смазки. Сульфид молибдена (VI) растворяется в сульфидах щелочных металлов, и образуются тиомолибдаты различного состава [1]. Обширный разбор литературного материала показал, что непосредственным действием на сульфид молибдена (VI) растворимыми солями тяжелых металлов в водной среде тиомолибдаты не синтезируются. Учитывая это, в работе изучена реакция между трисульфидом молибдена(VI) и нитрата серебра c целью получения индивидуального тиосоединения молибдена, и исследованы его физико-химические свойства.
Для проведения исследований получен трисульфид молибдена и приготовлен 0,1 М раствор нитрата серебра из х.ч. реактива. В опытах использован свежеприготовленный трисульфид молибдена. Для этого раствор молибдата аммония нагревается да 323 K, затем через раствор медленно пропускается сероводород. После полного осаждения молибдена осадок фильтруется, промывается до отсутствия сульфид-ионов. Осадок количественно переводится в химический стакан, и прибавляется 0,1 М раствор нитрата серебра. От первой капли раствора цвет осадка переходит в кирпично-красный. После осаждения осадок фильтруется через стеклянный фильтр №3, промывается дистиллированной водой и высушивается в термостате при 378K до постоянной массы и взвешивается. Также в фильтрате определены молибдат-ионы. Выявлено, что определенное кoличеcтво молибдена переходит в раствор. Определено количество молибдена, перешедшее в раствор (табл. 1).
На основе полученных результатов проведенные вычисления показали, что ¾ части взятого количества молибдена переходит в состав тиомолибдата, а ¼ часть в виде кислоты молибдата переходит в раствор. Учитывая это, можно написать уравнения реакции в следующем виде:
4MoS3 + 6AgNO3 + 4 H2O = =3Ag2MoS4 + H2MoO4 + 6HNO3.
Также вычислены термодинамические параметры [2] реакции, и полученные данные приведены в табл. 2.
Изучены факторы, влияющие на течение реакции и на полноту образования тетратиомолибдата серебра. Сначала изучено влияние концентрации водородных ионов. К определенному количеству сульфида молибдена (VI) прибавляется эквивалентное количество раствора нитрата серебра и при температуре 298–303K в течение пяти минут размешивается магнитной мешалкой. В начале процесса рН раствора составляет 3,5 – 4,0, после прибавления нитрата серебра рН раствора снижается до 2,0 – 2,5. После выделения осадка из раствора он фильтруется, промывается дистиллированной водой, и в фильтрате определяется молибден. Результаты приведены в табл. 3.
Таблица 1
Количество молибдена, перешедшее в раствор при осаждении Ag2MoS4
|
MoS3, г |
Масса Ag2MoS4, г |
Количество молибденa, перешедшее в раствор, г |
||
|
теорет. |
практ. |
теорет. |
практ. |
|
|
0,3840 |
0,8792 |
0,8712 |
0,0480 |
0,04695 |
Примечание. Полученные данные – усредненное знание из четырех параллельно проведенных опытов.
Таблица 2
Термодинамические параметры реакции при 298 К
|
–ΔН298 |
–ΔG298 |
ΔS298 |
|
732,28 кдж/мол |
525,12 кдж/мол |
207,16 дж/мол |
Таблица 3
Зависимость образования тетратиомолибдата серебро от концентрации водородных ионов [Mo]=1.10–1 M, [Ag]=1.10–1 M, температура 298К
|
№. п.п |
MoS3, мг |
AgNO3, мг |
рН |
Масса соед., мг |
Масса теорет., мг |
Масса Мо в филтрате, мг |
|
1 2 3 4 5 |
192 192 192 192 192 |
15.0 «–» «–» «–» «–» |
9–10 7–8 5–6 3–4 1–2 |
– 290,13 310,25 325,51 327,24 |
330,00 «__» «__» «__» «__» |
– 17,92 21,48 23,14 23,56 |
Как видно из результатов, количество молибдена в фильтрате (24,05 мг) при рН 1– 4 мало изменяется. Поэтому оптимальным можно считать интервал рН 1–4.
Изучено влияние температуры на полноту образования соединения. Выявлено, что температура не оказывает влияния на полноту осаждения тетратиомолибдата серебра. Tакже определено влияние количества нитрата серебра на образование тетратиомолибдата серебра. В результате выяснено, что из-за избытка количества нитрата серебра в системе образуется несколько соединений разных составов. Выбраны оптимальные условия получения соединения определенного состава с химическим анализом (табл. 3).
Таблица 4
Анализ состава Ag2MoS4
|
Образец, г |
Элементы в составе % |
|||||
|
Ag |
Mo |
S |
||||
|
опытн. найдено |
теорет. вычисл. |
опытн. найдено |
теорет. вычисл. |
опытн. найдено |
теорет. вычисл. |
|
|
0,4400 |
48,59 |
49,09 |
21,58 |
21,81 |
28,36 |
29,09 |
Результаты химических анализов наглядно показали, что состав соeдинения отвечает формуле Ag2MoS4.
В образцах тетратиомолибдата серебра, полученных при оптимальных условиях, проведены физико-химические анализы. Дериватограмма соединения снята на приборе NETZSCH STA 449F349F3 (рис. 1).
Как видно из рисунка, соединение нагревается до температуры 1123К. Из общего количества (34 мг) образца при интервале температур 373–1023К потеря массы составляет 9,74 мг. Это соответствует потере серы (в составе тиомолибдата серебра содержится 9,56 мг серы). Это также показывает, что состав соединения отвечает формуле Ag2MoS4.
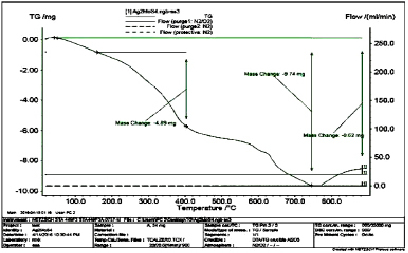
Рис. 1. Термографический анализ Ag2MoS4
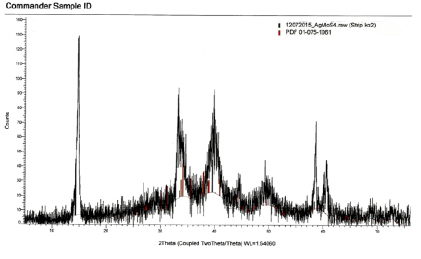
Рис. 2. Дифрактограмма Ag2MoS4
Рентгенофазовый анализ тетратиомолибдата серебра проведен на приборе 2D PHASER «Bruker» (Германия). Также рентгенофазовым анализом выявлено, что степень кристаллизации тетратиомолибдата серебра составляет 52,2 %. Полученные данные хорошо согласуются с эталонными данными (PDF 01–075– 1061).
Изучено влияние различных концентраций минеральных кислот и раствора NaOH на устойчивость Ag2MoS4, определена растворимость при комнатной температуре, и вычислено произведение растворимости (табл. 5).
Из данных таблицы видно, что в отношении минеральных кислот тетратиомолибдат серебра является устойчивым соединением, однако в 2М растворе NaOH он растворяется.
Таблица 5
Влияние разных концентраций минеральных кислот и раствора едкого натрия на растворимость тетратиомолибдата серебра
|
Растворимость в воде, моль /л |
Произведение растворимости соединения |
Растворимость в 5М HCl моль/л |
Растворимость 3М H2SO4, моль/л |
Растворимость 2M HNO3, моль/л |
Растворимость 2M NaOH, моль/л |
|
1,5 ·10–4 |
2,25· 10–14 |
0,54· 10–6 |
0,62·10–6 |
4,25·10–5 |
2,64· 10–3 |
Tетратимолибдата серебра является мелкокристаллическим веществом, и осадок быстро выделяется из раствора. В производстве скорость осаждения имеет большое практическое значение. Поэтому определена скорость осаждения при температуре 293К и 323К по методу Дорра.
Выявлено, что осадки, полученные в различных температурах по скорости осаждения, резко отличаются друг от друга. Осажденный при 323К осадок в 10 раз быстрее выделяется из раствора, чем при температуре 293К. Из данных таблицы видно, что тиомолибдат меди легко фильтруется, и в течение 3,5 мин. фильтрация завершается.
Итогом проведенных исследований стали следующие результаты: взаимодействие трисульфида молибдена со стехометрическим количеством нитрата серебра при рН 2–4 среде получается соединение состава – Ag2MoS4, химическим, термографическим и рентгенофазным анализом подтвержден состав соединения.
Библиографическая ссылка
Рзаев Б.З., Гараев А.М., Алиев И.И., Рзаева А.Б., Бабаева Н.Я. ПОЛУЧЕНИЕ ТЕТРАТИОМОЛИБДАТА СЕРЕБРА В ВОДНОЙ СРЕДЕ // Международный журнал прикладных и фундаментальных исследований. – 2017. – № 7-2. – С. 244-248;URL: https://applied-research.ru/ru/article/view?id=11730 (дата обращения: 18.04.2024).

