Как известно, при смешивании водных растворов двух полимеров при определенных концентрациях компонентов смеси расслаиваются на две жидкие фазы. Впервые это явление было обнаружено в работе [1]. В дальнейшем стало известно, что существуют также другие пары полимеров, которые термодинамически не совместимы в одном общем растворителе (воде), и выше определенных концентраций этих полимеров системы разделяются на две фазы [2]. Исследование водорастворимых полимеров в общем растворителе подтвердило, что фазовое расслоение в смесях полимеров в воде явление обычное [3] и растворителем в обеих фазах, является вода, при этом её содержание в каждой из фаз может составлять 70 и более процентов, а каждая из фаз системы обогащена одним из полимеров.
Следует отметить, что несовместимость компонентов в общем растворителе (воде) может иметь место и в водных смесях полимера с неорганической или органической солями, например, в системах ПЭГ-некоторые соли [4].
Впервые водные двухфазные системы, образуемые двумя несовместимыми парами полимеров, были систематически исследованы Альбертсоном, результаты которых были представлены в виде монографии [5]. Метод неравномерного распределения вещества в двухфазных водно-полимерных системах, который применен в работе [5], позволил осуществить разделение и очистку биологических материалов различной природы (белков, нуклеиновых кислот, клеточных органелл, вирусов, бактерий и т.д.).
В последнее время для разделения и очистки различных веществ и фракционирования высокомолекулярных соединений широко используют водные двухфазные системы «полимер-вода-соль». В качестве соли используют как неорганические, так и органические соли. Такие системы отличаются сравнительно высокой скоростью разделения и значительной дешевизной используемых материалов. Роль исследования водных двухфазных систем и метода распределения веществ в таких системах значительно возросла после того, как в работе [6] были показаны возможности этого метода для оценки относительной гидрофобности водных растворов различных веществ, очень важного параметра, определяющего процесс расслоения, а также возможности направленного регулирования разделительной способности этих водных двухфазных систем (полимер-полимер-вода; полимер-соли-вода).
Согласно развиваемым в последнее время представлениям основой возникновения разделительных свойств, определяемых разницей в свойствах сосуществующих фаз водных двухфазных систем, являются различия в структуре воды равновесных фаз системы.
Поскольку вода в таких сложных системах находится под воздействием многих факторов (температура, природа фазообразующих компонентов, различные добавки, молекулярно-массовое распределение полимерного компонента системы и т.д.), изучение влияния этих факторов, как в отдельности, так и совместно на структуру воды и, соответственно, на свойства водных двухфазных систем очень важно для понимания механизма расслоения системы на две фазы и управления разделительной способностью таких систем. Для описания водных двухфазных систем принято использовать фазовые диаграммы (бинодальние кривые, соединительные линии и т.д.) этих систем, где на оси ординат откладываются содержание одного полимера (в весовых концентрациях), на оси абсцисс содержание другого полимера или соли. Важное значение имеет, как с практической, так и с теоретической точек зрения исследование влияния различных веществ на фазовые диаграммы водных двухфазных систем.
Нами было изучено влияние некоторых одноатомных спиртов (метанол, этанол, пропанол) на фазовую диаграмму водной двухфазной системы «ПЭГ-натриевая соль лимонной кислоты-вода»).
Впервые водно-двухфазные системы на основе ПЭГ-органические соли и влияние различных факторов на фазовые диаграммы этих систем исследовано в работе [8]. Полученные результаты по влиянию спиртов на фазовую диаграмму двухфазной системы ПЭГ-натриевая соль лимонной кислоты-вода представлены на рис.1. Как следует из рисунков бинодали фазовой диаграммы в присутствии метанола и этанола смещены в сторону увеличения гомогенной области диаграммы, причем такое смещение тем меньше, чем больше число гидрофобных функциональных групп в молекуле спирта. Как следует из рисунков, в присутствии пропанола (CH3CH2CH2OH) число гидрофобных групп равно трем, бинодали смещены в сторону увеличения гетерогенной области фазовой диаграммы.
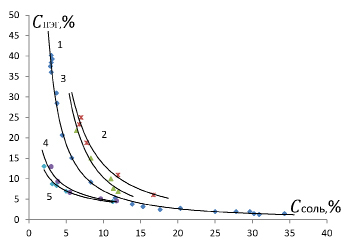
Влияние некоторых спиртов на фазовую диаграмму двухфазной систем «ПЭГ-натриевая соль лимонной кислоты-вода»: 1 – основная бинодаль; 2 – метанол; 3 – этанол; 4 – пропанол (0,3 мол/л); 5– пропанол (0,5 мол/л)
Полученные результаты можно попытаться объяснить следующим образом. Фазообразующие компоненты системы – ПЭГ и натриевая соль лимонной кислоты в какой-то мере структурируют воду. В этом не малую роль играют ионы натрия диссоциированной соли, которые блокируют атомами кислорода молекулы полиэтиленгликоголя, тем самым отключая водородные связи этого кислорода с молекулами воды. При присутствии спиртов, их гидроксильные группы, входя в водородную связь с молекулами воды в некоторой степени разрушают структуру воды, что приводит к улучшению совместимости фазообразующих компонентов. Однако гидрофобные функциональные группы спиртов естественно структурирует воду, уменьшая частоты обмена между молекулами воды, связанными с молекулами спиртов, и между объемными молекулами воды. Этот процесс приводит к ухудшению совместимости фазообразующих компонентов. Первый из этих процессов, т.е. возникновение водородных связей между гидроксильными группами спиртов и молекулами воды, разрушая структуру воды, приводит к улучшению совместимости фазообразующих компонентов, а второй процесс за счет гидрофобной гидратации неполярных функциональных групп спиртов приводит к ухудшению совместимости фазообразующих компонентов двухфазной системы. В конкуренции этих двух процессов, как показывают результаты экспериментов, превалирует сначала разрушающее структуру воды влияние гидроксильных групп спиртов, затем с увеличением гидрофобных групп спиртов влияние этих групп компенсирует влияние OH- групп и в дальнейшем превосходит влияние единственной гидроксильной группы спиртов. Об этом свидетельствует также увеличение смещения бинодали под влиянием пропилового спирта с ростом его концентрации.
Библиографическая ссылка
Масимов Э.А., Шахбазова Г.М., Багиров Т.О., Оджагвердиева С.Я. ВЛИЯНИУ НЕКОТОРЫХ ОДНОАТОМНЫХ СПИРТОВ НА ФАЗОВУЮ ДИАГРАММУ «ПЭГ-НАТРИЕВАЯ СОЛЬ ЛИМОННОЙ КИСЛОТЫ-ВОДА» // Международный журнал прикладных и фундаментальных исследований. – 2017. – № 9. – С. 140-142;URL: https://applied-research.ru/ru/article/view?id=11843 (дата обращения: 25.04.2024).

