Внедрение международных отраслевых стандартов в фармацевтической отрасли является актуальной задачей. Требования перехода аптечных организаций на стандарты GPP (Good Pharmacy Practice) с 1 марта 2017 г. законодательно закреплены в приказе МЗ РФ № 647н от 31.08.2016 г. «Об утверждении Правил надлежащей аптечной практики лекарственных препаратов для медицинского применения». В связи с этим одной из основных проблем для аптек, осуществляющих изготовление лекарственных препаратов, является разработка стандартных операционных процедур (СОПов) – внутренних нормативных документов, регламентирующих все виды деятельности аптечной организации. Основной задачей СОПов является предупреждение совершения ошибок при выполнении той или иной манипуляции. Созданная в аптеке СОП должна быть подробной и четкой пошаговой инструкцией, реально отражающей все виды деятельности сотрудника аптеки в конкретной ситуации. СОПы могут быть дополнены инструкциями, расположенными рядом с рабочими местами сотрудников, и помочь конкретизировать каждый этап той или иной процедуры. СОП может быть составлена в виде обычного текста или в виде таблицы, схемы последовательных процедур [1].
Таким образом, стандартная операционная процедура (СОП) – это документально оформленные локальные нормативные правовые акты аптечной организации, содержащие детальное описание стадий процедуры (способа или процесса), которые должны быть выполнены с соблюдением требований действующего законодательства, регулирующего осуществление фармацевтической деятельности, а также мер предосторожности, прямо или косвенно относящихся к изготовлению, контролю качества и (или) реализации лекарственных средств [2].
Производственная деятельность аптеки невозможна без использования воды очищенной. Вода в аптеках применяется для разных целей: в качестве растворителя при производстве лекарственных средств, вспомогательного вещества в составе лекарственных препаратов, для мойки, обработки и очистки оборудования и т.д. Поэтому контролю качества воды в аптеках уделяется особое внимание, и, соответственно, одной из основных профессиональных задач провизора-аналитика является контроль качества воды очищенной.
В связи с этим целью данного исследования явилась разработка алгоритма составления стандартной операционной процедуры (СОП) – контроль качества воды очищенной в условиях аптечных организаций, осуществляющих изготовление и отпуск лекарственных препаратов для медицинского применения.
Материалы и методы исследования
Алгоритм составления СОП по контролю качества воды очищенной разработан согласно требованиям ФС.2.2.0020.18 «Вода очищенная» ГФ РФ XIV издания и в соответствии с действующей нормативной документацией, регламентирующей деятельность аптечных организаций [3].
Результаты исследования и их обсуждение
Разработанный алгоритм составления стандартной операционной процедуры по контролю качества воды очищенной в условиях производственных аптек включает несколько разделов (рисунок).
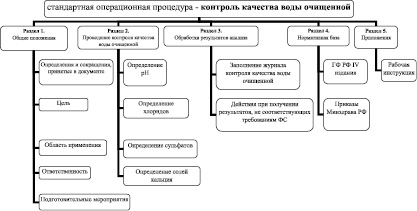
Содержание разделов СОП по контролю качества воды очищенной
Титульный лист документа может содержать графы, представленные в табл. 1.
Таблица 1
Титульный лист СОП по контролю качества воды очищенной
|
Название СОП: Контроль качества воды очищенной |
|
|
Наименование аптечной организации ____________________________________________ |
|
|
Код (номер) документа: |
|
|
Составил: Провизор-аналитик____________ ____________ Ф.И.О. подпись |
Утвердил: Руководитель ___________________ __________ Ф.И.О. подпись |
|
Документ введен в действие: «___» _____ 20___г |
Документ актуализирован: «___» _____ 20___г |
Раздел 1. Общие положения
Определения и сокращения, принятые в документе
1. ГФ – Государственная фармакопея.
2. ФС – Фармакопейная статья.
3. ОФС – Общая фармакопейная статья.
4. СОП – Стандартная операционная процедура.
Цель: стандартизация процедуры контроля качества воды очищенной.
Область применения: настоящая стандартная операционная процедура определяет порядок анализа воды очищенной и форму отчетности.
Ответственность: положения, изложенные в данной стандартной операционной процедуре (СОП) обязательны для провизора-аналитика.
Подготовительные мероприятия и общие замечания к проведению контроля качества воды очищенной:
1. Подготовка приборов и оборудования:
В качестве прибора для потенциометрического определения рН используют иономеры или рН-метры с чувствительностью не менее 0,05 единиц рН или 3 мВ [4].
2. Подготовка реактивов для контроля качества одной пробы воды очищенной [5]:
1) насыщенный раствор калия хлорида 0,3 мл;
2) раствор кислоты азотной 0,5 мл;
3) 2 % раствор серебра нитрата 0,5 мл;
4) 7,3 % раствор кислоты хлористоводородной разведенной 0,1 мл;
5) 6,1 % раствор бария хлорида 0,1 мл;
6) 10 % раствор аммония хлорида 1 мл;
7) 10 % раствор аммиака 1 мл;
8) 4 % раствор аммония оксалата 1 мл.
3. Подготовка лабораторной посуды, необходимой для контроля качества одной пробы воды очищенной:
1) стакан лабораторный 100 мл.
2) пробирки бесцветные, прозрачные, из нейтрального стекла с плоским дном, одинакового диаметра (около 1,5 см), 6 штук;
3) пипетки мерные градуированные 1 мл, 6 штук;
4) микропипетки мерные градуированные, 2 штуки;
5) пробоотборник, изготовленный из материала, который не загрязняет воду и не реагирует с ней. Вместимость пробоотборника должна быть достаточной для отбора всей точечной пробы, а его конструкция должна быть доступна для очистки. Используемые пробоотборники должны быть чистыми и сухими.
4. Процедура отбора проб воды очищенной [6]:
Отбор проб осуществляет провизор-аналитик ежедневно из каждого баллона в количестве 130 мл (для контроля качества одной пробы); при подаче воды по трубопроводу – на каждом рабочем месте в количестве 130 мл (для контроля качества одной пробы).
Отбор точечных проб проводят пробоотборником с разных уровней: верхнего, среднего и нижнего слоев каждого баллона (крана трубопровода). Для отбора проб воды очищенной ее сначала тщательно перемешивают; в случае, если перемешивание затруднено (большие емкости), точечные пробы отбирают без перемешивания из разных слоев.
5. Общие замечания:
Согласно требованиям приказа Мин- здрава РФ № 751н от 26.10.2015 «Об утверждении правил изготовления и отпуска лекарственных препаратов для медицинского применения аптечными организациями, индивидуальными предпринимателями, имеющими лицензию на фармацевтическую деятельность», разделу VII, п.130 вода очищенная ежедневно из каждого баллона проверяется на отсутствие хлоридов, сульфатов и солей кальция в соответствии с требованиями действующей Государственной фармакопеи XIV издания и ФС.2.2.0020.18 «Вода очищенная».
Ежеквартально вода очищенная должна направляться в аккредитованную в установленном порядке испытательную лабораторию (центр) для полного анализа в соответствии с требованиями Государственной фармакопеи и иных, утвержденных в установленном порядке нормативных правовых актов. Отбор проб и их предоставление на анализ в сторонние лаборатории, а также получение результатов анализа осуществляет провизор-аналитик.
Раздел 2. Проведение контроля качества воды очищенной
1. Методика определения рН в воде очищенной:
Определение проводят потенциометрически в соответствии с требованиями ОФС.1.2.1.0004.15 «Ионометрия». В ФС.2.2.0020.18 «Вода очищенная» ГФ РФ XIV отсутствует значение показателя рН, однако согласно требованиям приказа Минздрава РФ № 751н от 26.10.2015 провизор-аналитик при заполнении журнала регистрации контроля качества воды очищенной должен внести результаты определения рН в соответствующую графу. В связи с этим необходимо определить значение этого показателя. Подготовка приборов к работе и проведение измерений производят согласно прилагаемым инструкциям. Измерения проводят при температуре в интервале от 20 до 25 °С. К 100 мл испытуемой воды очищенной прибавляют 0,3 мл насыщенного раствора калия хлорида. Электроды прибора погружают в испытуемый раствор и измеряют рН. Полученные результаты провизор-аналитик вносит в журнал регистрации результатов контроля воды очищенной.
2. Методика проведения испытания на недопустимые примеси в воде очищенной [7].
Хлориды (Cl-) [8]:
Методика: к 10 мл испытуемой воды очищенной прибавляют 0,5 мл азотной кислоты, раствор делят на две равные части (пробирки одинакового стекла и диаметра). В одну из пробирок прибавляют 0,5 мл 2 % раствора серебра нитрата, перемешивают и через 5 мин пробирки просматривают на темном фоне в проходящем свете. Между пробирками не должно быть заметной разницы.
Химизм реакции:
Cl- + AgNO3 → AgCl + NO3-
Наблюдаемый результат _____________.
Вывод: вода очищенная соответствует/не соответствует требованиям по содержанию хлоридов.
Сульфаты (SO42-) [9]:
Методика: к 10 мл испытуемой воды очищенной прибавляют 0,1 мл 7,3 % раствора кислоты хлористоводородной разведенной, раствор делят на две равные части (пробирки одинакового стекла и диаметра). В одну из пробирок прибавляют 0,1 мл 6,1 % раствора бария хлорида, перемешивают и через 1 час пробирки просматривают на темном фоне в проходящем свете. Между пробирками не должно быть заметной разницы.
Химизм реакции:
SO42- + BaCl2 → BaSO4 + 2Cl-
Наблюдаемый результат _____________.
Вывод: вода очищенная соответствует/не соответствует требованиям по содержанию сульфатов.
Кальций (Ca2+) [10]:
Методика: к 10 мл испытуемой воды очищенной прибавляют 1 мл 10 % раствора аммония хлорида, 1 мл 10 % раствора аммиака, раствор делят на две равные части (пробирки одинакового стекла и диаметра). В одну из пробирок прибавляют 1 мл 4 % раствора аммония оксалата, перемешивают и через 10 мин пробирки просматривают на темном фоне в проходящем свете. Между пробирками не должно быть заметной разницы.
Химизм реакции:
Ca2++ (NH4)2C2O4 →CaC2O4+2(NH4)+
Наблюдаемый результат _____________.
Вывод: вода очищенная соответствует/не соответствует требованиям по содержанию ионов кальция.
Раздел 3. Обработка результатов анализа
По результатам проведенных испытаний провизор-аналитик заполняет журнал регистрации результатов контроля воды очищенной согласно требованиям приказа Минздрава РФ № 751н от 26.10.2015 г. Графы журнала представлены в табл. 2.
Таблица 2
Форма журнала контроля качества воды очищенной
|
дата получения (отгонки) воды |
дата контроля воды |
номер проведенного химического анализа |
номер баллона или бюретки, из которых взята на анализ вода |
результаты контроля на отсутствие примесей |
показатели рН среды |
заключение о результатах анализа воды (удовлетворяет/не удовлетворяет) |
подпись лица, проводившего анализ |
|
1. |
2. |
3. |
4. |
5. |
6. |
7. |
8. |
Журнал регистрации результатов контроля воды очищенной должен быть пронумерован, прошнурован и скреплен подписью руководителя учреждения и печатью вышестоящей организации.
При получении результатов анализа воды очищенной, не соответствующих требованиям ФС, получают новую партию воды очищенной и проводят контроль качества полученной воды.
Раздел 4. Нормативная база, используемая при создании СОП
1. Государственная фармакопея Российской Федерации XIV издания. Том 3. – М., 2018. – ФС.2.2.0020.18. «Вода очищенная».
2. Приказ МЗ РФ от 26.10.2015 г. № 751н «Об утверждении правил изготовления и отпуска лекарственных препаратов для медицинского применения аптечными организациями, индивидуальными предпринимателями, имеющими лицензию на фармацевтическую деятельность». – М., 107 с.
Раздел 5. Приложения к СОП
Приложения содержат рабочую инструкцию, содержащую краткое изложение проводимых испытаний (табл. 3). Рабочая инструкция размещается непосредственно на рабочем месте провизора-аналитика.
Таблица 3
Рабочая инструкция по контролю качества воды очищенной
|
Определяемый показатель |
Методика проведения испытания |
Результат |
|
рН |
К 100 мл испытуемой воды очищенной + 0,3 мл насыщенного раствора калия хлорида, измеряют рН потенциометрически |
рН от 5,0 до 7,0 |
|
Хлориды |
В пробирку 10 мл испытуемой воды очищенной + 0,5 мл азотной кислоты, раствор делят на две равные части (пробирки одинакового стекла и диаметра). В одну из пробирок + 0,5 мл 2 % раствора серебра нитрата, перемешивают и через 5 мин пробирки просматривают на темном фоне в проходящем свете |
Различий между пробирками быть не должно |
|
Сульфаты |
В пробирку 10 мл испытуемой воды очищенной + 0,1 мл 7,3 % раствора кислоты хлористоводородной разведенной, раствор делят на две равные части (пробирки одинакового стекла и диаметра). В одну из пробирок + 0,1 мл 6,1 % раствора бария хлорида, перемешивают и через 1 час пробирки просматривают на темном фоне в проходящем свете |
Различий между пробирками быть не должно |
|
Кальций |
В пробирку 10 мл испытуемой воды очищенной + 1 мл 10 % раствора аммония хлорида, 1 мл 10 % раствора аммиака, раствор делят на две равные части (пробирки одинакового стекла и диаметра). В одну из пробирок + 1 мл 4 % раствора аммония оксалата, перемешивают и через 10 мин пробирки просматривают на темном фоне в проходящем свете |
Различий между пробирками быть не должно |
|
Заключение |
Заполняют журнал регистрации результатов контроля воды очищенной |
удовлетворяет/ не удовлетворяет |
Заключение
Таким образом, разработанный алгоритм составления СОП по контролю качества воды очищенной может быть использован сотрудниками производственных аптек в качестве шаблона при разработке собственных СОПов.
Библиографическая ссылка
Савченко И.А., Корнеева И.Н., Лукша Е.А., Подгурская В.В. РАЗРАБОТКА СТАНДАРТНОЙ ОПЕРАЦИОННОЙ ПРОЦЕДУРЫ «АНАЛИЗ ВОДЫ ОЧИЩЕННОЙ В УСЛОВИЯХ АПТЕЧНЫХ ОРГАНИЗАЦИЙ, ОСУЩЕСТВЛЯЮЩИХ ИЗГОТОВЛЕНИЕ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ» // Международный журнал прикладных и фундаментальных исследований. – 2018. – № 11-2. – С. 305-309;URL: https://applied-research.ru/ru/article/view?id=12495 (дата обращения: 27.04.2024).

