Среди опухолей головы и шеи рак гортани составляет – 65-70 % [2]. В соответствии с современными стандартами, лечение больных плоскоклеточным раком гортани (ПРГ) должно проводиться в виде комплекса мероприятий с применением хирургического метода, лучевого лечения и химиотерапии [3]. Индукционная химиотерапия позволяет выбрать пациентов с опухолями, чувствительными к дальнейшему лечению, с последующим проведением минимально калечащих хирургических вмешательств на ранних этапах [1, 5, 6].
Появление таргетных препаратов открыло новый этап в лечении пациентов с ПРГ. Известно, что при плоскоклеточном раке головы и шеи, и в частности, при ПРГ, экспрессируется рецептор эпидермального фактора роста (РЭФР), повышение его экспрессии обычно ассоциируется со снижением безрецидивной и общей продолжительности жизни [4]. Таким образом, мишенью при лечении указанной категории больных становится РЭФР. К препаратам, воздействующим на рецептор эпидермального фактора роста, относится цетуксимаб – представитель высокоактивных моноклональных антител класса IgG, механизм действия которого, в отличие от стандартной неселективной химиотерапии, заключается в его избирательном воздействии на РЭФР и связывании с ним. Такое связывание предотвращает активацию рецептора и передачу сигнала по его сигнальному пути, и в свою очередь, приводит к угнетению инвазии опухолевых клеток в нормальные ткани и препятствует распространению опухоли в другие органы. Считается, что препарат также угнетает способность опухолевых клеток исправлять повреждения после химио- и лучевой терапии, а также подавляет процесс образования новых кровеносных сосудов в толще опухоли, что приводит к общему угнетению опухолевого роста [7]. Результаты ряда крупных рандомизированных международных клинических исследований продемонстрировали эффективность включения цетуксимаба в схемы лечения больных с рецидивным и/или метастатическим плоскоклеточным раком головы и шеи [9]. Получены данные об увеличении медианы выживаемости больных без прогрессирования болезни почти в два раза при добавлении цетуксимаба к полихимиотерапии с использованием цисплатина и 5-фторурацила [10]. В доступной литературе недостаточно данных о влиянии цетуксимаба на показатели периферической крови.
Цель данного исследования – оценка эффективности применения комбинации цетуксимаб/цисплатин + 5-фторурацил у больных плоскоклеточным раком гортани.
Материалы и методы исследования
В исследование включены 41 больной с гистологически верифицированным ПРГ различной степени дифференцировки, I-III стадии в возрасте 55-68 лет. Из них 14 (34,1 %) – пациенты с местно-распространенным процессом, 27 (65,9 %) – с рецидивами рака гортани, получивших лечение в РНИОИ в период 2015-2016 годы. Все больные раком гортани были лицами мужского пола. 20 пациентов (основная группа) получили противоопухолевое лечение по схеме: цетуксимаб в дозе 400 мг/м2поверхности тела в/в капельно в 1-й день лечения, далее по 250 мг/м2 в/в капельно в 8-й и 15-й дни; цисплатин в дозе 100 мг/м2 в/в капельно в 1- день; 5-фторурацил – по 500 мг/м2 в/в капельно во 1 – 4-й дни (96-ти часовая инфузия). 21 пациент ПРГ (контрольная группа) получили по аналогичной схеме цисплатин, 5-фторурацил, но без цетуксимаба. Каждому больному после завершения запланированного неоадьювантного курса ПХТ с цетуксимабом была выполнена фиброларингоскопия для оценки результатов лечения.
Исследованы: суммарный показатель лейкоцитов – WBC, количество незрелых гранулоцитов – IG, нейтрофилы – Ne, лимфоциты – Ly и моноциты – Mo (Sysmex XE 2100, Япония), С-реактивный белок (СРБ), лактатдегидрогеназа (ЛДГ), креатинин (Cobas Integra Plus, Швейцария). Исследования проведены до-, во 2-й, 9-й, 16-й дни и после окончания лечения.
Статистический анализ результатов исследований проводили с использованием пакета программ Statistiсa 6.0. Различия считали статистически значимыми при p < 0,05 – p < 0,001, а при 0,1 > p > 0,05 – на уровне статистической тенденции.
Результаты исследования и их обсуждение
Для оценки ответа на лечение использованы критерии эффекта по шкале RECIST, версия 1.1 [8]. Согласно данным у 16 (80,0 %) больных ПРГ основной группы получен частичный ответ, у 4 (20,0 %) – стабилизация процесса (табл. 1). В контрольной группе частичный ответ отмечен у 5 (23,8 %) больных, стабилизация опухолевого процесса – у 12 (57,4 %), прогрессирование заболевания – у 4 (19,0 %).
Таблица 1
Непосредственные результаты лечения больных ПРГ по RECIST, n ( %)
|
Лечебный эффект |
Основная группа n = 20 |
Контрольная группа n = 21 |
|
Полный ответ |
– |
– |
|
Частичный ответ |
16 (80,0) |
5 (23,8) |
|
Стабилизация |
4 (20,0) |
12 (57,2) |
|
Прогрессирование |
– |
4 (19,0) |
У 10 из 16 больных основной группы с частичным ответом на лечение комбинацией цетуксимаб/цисплатин+5-фторурацил, после каждого введения цетуксимаба отмечено увеличение общего количества лейкоцитов в 1,8-2,0 раза в сравнении со значениями до начала лечения. Так, после 1-го введения препарата количество WBC составило 13,40 ± 2,86×109/л, после 2-го -13,52 ± 1,88×109/л, после 3-го – 12,25 ± 2,08×109/л (табл. 2).
Таблица 2
Динамика показателей лейкоцитарного звена периферической крови на этапах лечения больных ПРГ по схеме цетуксимаб/цисплатин + 5-фторурацил
|
Исследуемые показатели ×109/л |
Этапы обследования |
||||
|
до лечения |
2-й день |
9-й день |
16-й день |
Конец лечения |
|
|
WBC |
6,87 ± 1,45 |
13,40 ± 2,86 p < 0,001 |
13,52 ± 1,88 p < 0,001 |
12,25 ± 2,08 p < 0,01 |
5,27 ± 0,72 |
|
Ne×109/л % |
3,84 ± 0,53 55,9 ± 5,65 |
10,13 ± 0,99 75,6 ± 5,49 p < 0,001 |
10,34 ± 1,15 76,5 ± 3,94 p < 0,001 |
10,06 ± 0,44 82,2 ± 2,04 p < 0,001 |
3,49 ± 0,38 66,23 ± 4,32 |
|
IG×109/л % |
0,014 ± 0,01 0,21 ± 0,014 |
0,044 ± 0,021 0,32 ± 0,089 p < 0,001 |
0,056 ± 0,015 0,44 ± 0,055 p < 0,001 |
0,060 ± 0,008 0,50 ± 0,022 p < 0,001 |
0,037 ± 0,021 0,60 ± 0,026 р < 0,01 |
|
Ly×109/л % |
2,18 ± 0,45 31,72 ± 4,62 |
2,49 ± 1,48 18,6 ± 4,48 |
2,24 ± 0,58 16,65 ± 5,37 |
1,56 ± 0,60 12,7 ± 4,24 p < 0,01 |
1,282 ± 0,19 24,32 ± 3,68 p < 0,01 |
|
Mo×109/л % |
0,56 ± 0,22 8,15 ± 2,82 |
0,734 ± 0,30 5,48 ± 2,34 |
0,805 ± 0,24 6,01 ± 1,91 |
0,588 ± 0,32 4,80 ± 0,84 |
0,882 ± 0,21 7,2 ± 1,71 |
Примечание. p – значимость различий по сравнению с исходными данными.
Отмеченный рост уровня WBC был обусловлен, преимущественно, увеличением абсолютного количества зрелых гранулоцитов (Ne) в среднем в 2,7 раза, а также, абсолютного и относительного количества IG фракции нейтрофилов в 3-4 раза (табл. 1). В соответствии с данными, абсолютное количество Ne и IG после 1-го, 2-го и 3-го введений цетуксимаба составило 10,13 ± 0,99×109/л, 10,34 ± 1,15×109/л, 10,06 ± 0,44×109/л и 0,044 ± 0,021×109/л, 0,056 ± 0,015×109/л, 0,060 ± 0,008×109/л, соответственно. Примечательно, что увеличение WBC и IG носило транзиторный характер: между точками оценки повышение уровня лейкоцитов и незрелых гранулоцитов сменялось их последовательным снижением до исходных значений и составило в среднем 7,21 ± 1,92×109/л (WBC) и 0,016 ± 0,002 ×109/л (IG). Возможно, это объяснимо минимальным токсическим воздействием комбинации цетуксимаб/цисплатин+5-фторурацил на предшественников гранулоцитопоэза, что способствует активации в ходе проводимой терапии гранулоцитопоэза. Подтверждением данного предположения может служить отсутствие лейкопений, а также – значимых изменений в содержании Mo и Ly, как на протяжении всего 2-х недельного полного курса ПХТ, так и по окончании цитостатического воздействия. Так, количество Мо находилось в пределах 0,60 – 0,80×109/л, отмечено умеренное снижение абсолютного содержания Ly на 16-й день лечения в среднем до 1,56 ± 0,60×109/л, которое к концу наблюдений составило 1,282 ± 0,19×109/л, то есть установилось на нижнем уровне референтного интервала.
У 6 из 16 пациентов основной группы с частичным ответом на лечение отмечались осложнения в виде кожной токсичности 1-2 степени. При этом общее состояние больных оставалось удовлетворительным, дополнительного лечения не требовалось. Обращало внимание отсутствие у этих больных повышения количества WBC. Отличий в содержании незрелых гранулоцитов (IG) в крови указанных пациентов основной группы от больных с эффектом от лечения (10 человек) без проявлений кожной токсичности не отмечено. По-видимому, отсутствие повышения суммарного показателя лейкоцитов (WBC) у пациентов с проявлением кожной токсичности может являться следствием ускоренного поступления лейкоцитов в ткани. Указанные изменения уровня лейкоцитов, как их повышение в процессе лечения, так и отсутствие такового, требуют, на наш взгляд, более длительных наблюдений.
Эффект от лечения по схеме цетуксимаб/цисплатин + 5-фторурацил сопровождался последовательным стойким снижением исходной концентрации СРБ (26,56 ± 5,63 mg/L) и креатинина (119,25 ± 15,4 umol/L) до уровня референтных значений (7,69 ± 3,28 mg/L и 74,75 ± 6,54 umol/L, соответственно) (рисунок). Концентрация ЛДГ (183,25 ± 24,76 U/L) не выходила за пределы референтного интервала на протяжении всего периода лечения. Полученные данные свидетельствуют об отсутствии у больных нарушений функции печени и почек, демонстрируют низкий общетоксический эффект ПХТ с цетуксимабом.
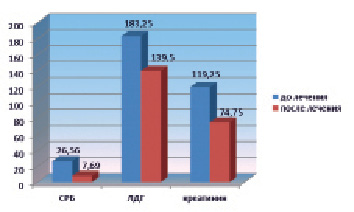
Уровень СРБ (mg/L), ЛДГ (U/L), креатинина (umol/L) до и после лечения больных основной группы с эффектом от лечения
При анализе лабораторных показателей 4-х больных основной группы со стабилизацией процесса и у 21 пациента контрольной группы, вне зависимости от результатов проведенной терапии, прослеживалась однонаправленность изменений исследуемых параметров. Отмечено умеренное снижение уровня WBC, который составил к концу лечения 3,90 ± 1,86×109/л и 3,84 ± 1,42×109/л соответственно, отсутствие положительной динамики в содержании незрелых гранулоцитов. Обращало внимание замедление темпов снижения концентрации СРБ, сохраняющейся к концу лечения у этих больных на уровне 12,60 ± 2,22 mg/L и 14,70 ± 3,52 mg/L соответственно, что превышало референтные значения (до 10,0 mg/L). Мы предполагаем, что это связано с выраженностью у больных интоксикационного синдрома, обусловленного отчасти самим заболеванием, отчасти – токсическим воздействием проведенной ПХТ. Таким образом, данные свидетельствуют, что комбинация цетуксимаб/цисплатин + 5-фторурацил обладает более эффективной противоопухолевой активностью и характеризуется хорошей переносимостью больными ПРГ, что делало возможным завершение лечения в запланированные сроки.
Выводы
1. Использование комбинации цетуксимаб/цисплатин + 5-фторурацил повышает эффективность лечения у больных плоскоклеточным раком гортани на неоадъювантном этапе терапии.
2. Цетуксимаб в комбинации с цисплатином и 5-фторурацилом обладает минимальным токсическим эффектом, о чем свидетельствует снижение в динамике лечения уровня СРБ, отсутствие изменений ЛДГ и креатинина.
3. Увеличение суммарного показателя лейкоцитов, сопряженное с увеличением абсолютного количества незрелых гранулоцитов свидетельствует об активации гранулоцитопоэза в условиях применения комбинации цетуксимаб/цисплатин+5-фторурацил в лечении больных ПРГ, и требует дальнейшего изучения.
Библиографическая ссылка
Гуськова Н.К., Владимирова Л.Ю., Рядинская Л.А., Енгибарян М.А., Донская А.К., Легостаев В.М., Торпуджян И.С., Аванесова К.А. ОПЫТ ПРИМЕНЕНИЯ ЦЕТУКСИМАБА В ЛЕЧЕНИИ БОЛЬНЫХ ПЛОСКОКЛЕТОЧНЫМ РАКОМ ГОРТАНИ // Международный журнал прикладных и фундаментальных исследований. – 2016. – № 4-5. – С. 913-916;URL: https://applied-research.ru/ru/article/view?id=9102 (дата обращения: 19.04.2024).

