Современные сельскохозяйственные производители направляют все усилия на получение максимальной прибыли. Эти агротехнические процессы базируются на использовании высокоэффективных технологий производства молока, мяса, сохранении племенного поголовья животных. Конъюнктура рынка требует ускоренное создание новых пород, линий, семейств высокопродуктивного скота. Мощным средством реализации поставленных задач стали искусственное осеменение, трансплантация эмбрионов, позволяющие значительно снизить генерационный интервал и ускорить оценку матерей, быков, обеспечить размножение животных с высокой генетической ценностью [1].
Важным является предупреждение потерь, обусловленных бесплодием и снижением уровня воспроизводства крупного рогатого скота. По данным специалистов Министерства сельского хозяйства республики Казахстан ежегодно сельскохозяйственные предприятия недополучают около 20 телят от каждых 100 коров и до 20 % годового удоя от каждой бесплодной коровы, преждевременно выбраковывают более 35 % коров и около 20 % первотелок [2]. Агропредприятия несут огромные экономические потери в результате снижения выхода телят, широкого распространения патологии родов и послеродового периода, увеличения бесплодия и яловости животных, продолжительности сервис-периода и межотельного периода, снижения уровня молочной продуктивности у проблемных коров. Экономические потери включают не только стоимость недополученных телят и молока, но и неоправданные затраты на кормление, содержание, уход и лечение проблемных коров, а также потери за счет преждевременной выбраковки высокоценных животных, которые можно предотвратить при экономически обоснованной организации работы по воспроизводству поголовья крупного рогатого скота [3, 5, 6]. Актуальность проблемы продиктована необходимостью поиска способов получения приплода с племенных животных, трансплантации эмбрионов для увеличения количества выхода телят. Целью настоящей работы являлось усовершенствование традиционного биотехнологического метода искусственного осеменения путем повышения эффективности трансплантации эмбрионов путем прямой пересадки без заморозки от коров-доноров к коровам-реципиентам.
Материалы и методы исследования
Экспериментальные исследования осуществлены на базе крестьянского хозяйства «Балке», расположенных на северо-западе Восточно-Казахстанской области, совместно со специалистами лаборатории ТОО «БиоПрофи» (г. Астана). При подборе доноров выделили группу племенных коров черно-пестрой породы (10 голов), у которых не отмечены осложнения (мертворождаемость, задержание последа, послеродовые заболевания половых органов), их индекс осеменения не превышал 1,5. Группу коров-реципиентов (10 голов) составили животные этого же хозяйства. Производителем являлся бык черно-пестрой породы Честер-220. Осеменение коров, биологический скрининг за их физиологическим состоянием, трансплантацию эмбрионов выполняли с соблюдением ветеринарно-санитарных правил и согласно действующей инструкции по искусственному осеменению коров и телок [3, 4]. В качестве среды для промывания использован фосфатно-буферный солевой раствор (ФБС) Дюльбекко, для вымывания зародышей из матки использованы катетер Фоллея с упругим мандреном и надувным баллончиком, предварительно простерилизованные. Стельность у самок – рецепиентов проверялись по уровню прогестерона в плазме крови на 21-й день, параллельно использовали ректальный метод с помощью аппарата ультразвуковой диагностики.
Результаты исследования и их обсуждение
Новые социально-экономические отношения требуют необходимости дальнейшего совершенствования крупного рогатого скота, порождают интерес к современным технологиям разведения, кормления и содержания животных. Одним из путей повышения эффективности отрасли, совершенствования скота на региональном уровне и отдельных хозяйств является воспроизводство и селекция высокопродуктивных животных.
В странах СНГ работы по пересадке эмбрионов животных и совершенствованию аспектов самого метода начаты в 70-х годах прошлого века. Современная технология трансплантации эмбрионов позволяет получить от коровы – рекордистки за ее жизнь несколько десятков телят. В США от одной коровы голштинской породы с выдающейся молочной продуктивностью получили 131 теленка. В одном из фермерских хозяйств США за 6 сборов от пяти коров заморозили 201 эмбрион, получили 113 телят. США, Канада, Англия, Новая Зеландия осуществляют экспорт эмбрионов в десятки стран мира [6, 7].
В регионах Восточного Казахстана молочное скотоводство – одна из главных животноводческих отраслей сельского хозяйства, продукцией которого является не только молоко, но и молодняк, который используется для собственного воспроизводства, племенной продажи, выращивания с последующей реализацией другим сельхозпредприятиям, откорма и реализации на мясо [2, 3]. Отобранные доноры являлись здоровыми коровами в возрасте от 3,5 до 7 лет с хорошо развитой молочной железой, пригодной к машинному доению. Ветеринарные специалисты ранее у них не фиксировали каких-либо осложнений родов и послеродового периода. Методом ректальной пальпации обследованы у коров-доноров состояние половых органов, чтобы исключить нарушения воспроизводительной функции, наличие кисты яичника, гипофункцию, воспаление яичниковой связки, эндометриты. По стандартной схеме выполнены работы по осеменению коров-доноров после регистрации суперовуляции. Зародыши извлечены у коров на 7-й день после осеменения. В ходе эксперимента нами модифицирована традиционная технологическая схема при трансплантации эмбрионов. Для извлечения эмбрионов нами выбран нехирургический способ, основанный на введении в матку особого зонда по естественному каналу. Зонд «Фоллея» имеет три канала. Один из каналов предназначен для надувания баллончика, который закупоривает рог матки, препятствуя вытеканию жидкости. По другому каналу вводится физиологический раствор (среда Дюльбекко) с температурой 25-30 °С, который вымывает эмбрионы и возвращается вместе с ними через третий канал зонда в пробирку, помещенную в водяную баню с температурой 35 °С. В этой жидкости из полости матки извлекаются эмбрионы (рис. 1). Закрепив катетер, промывали полость рога матки с помощью шприца Люэра вместимостью 50-60 мл. В рог матки в зависимости от его величины вводили порциями от 40-60 мл промывной жидкости, затрачивая на промывание каждого рога не более 500 мл. Наполнение матки промывной средой и степень ее оттока контролировали ректально.
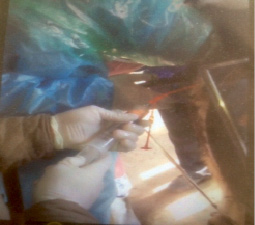
Рис. 1. Извлечение эмбрионов из полости матки с помощью зонда «Фоллея»
Некоторые авторы рекомендуют яйцепровод вблизи верхушки рога матки осторожно зажать большим и указательным пальцами. Видимо, при этом предотвращается поступление в брюшную полость жидкости, содержащей зародыши. Но практически у нас не отмечено поступление в брюшную полость жидкости из рога матки. Перед извлечением катетера следует удалить воздух из баллончика. Таким же образом промывали второй рог.
На рис. 2 показаны 7-дневные эмбрионы (при 10-кратном увеличении). В среднем при суперовуляции от донора были получены от 5 до 7 эмбрионов. Собранную в цилиндр промывную жидкость отстаивали 20-35 мин. при температуре 20-37 градусов, чтобы зародыши опустились на дно, после чего верхний слой удаляли с помощью сифона. Нижний слой жидкости порционно по 20-30 мл для обнаружения зародышей исследовали в специальных чашках Петри под бинокулярной лупой при 10-кратном увеличении. Найденных зародышей при помощи пастеровской пипетки переносили в среду для кратковременного хранения (среда Дюльбекко с добавлением 20 % фетальной сыворотки теленка). Как показали результаты исследований, полученные эмбрионы имели нормальное развитие, оказались пригодными для трансплантации реципиентам. Наблюдениями установлено, что обследованные эмбрионы находятся в стадии поздней морулы или бластоцисты. Морфологические структуры эмбрионов характеризуются компактностью, сферической формы. Клетки по размерам оказались примерно одинаковой величины, с гладкой, плоской и равномерно сформированной зоной пеллюцида, без включений в перивителлиновом пространстве. Эти эмбрионы полностью использованы для пересадки гормонально подготовленным коровам-реципиентам. После оценки зародышей их культивировали при 37 °С, пересадку эмбрионов произвели в течение 30 минут.
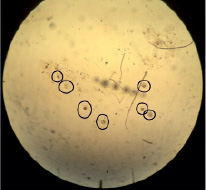
Рис. 2. Эмбрионы 7-дневного возраста, при 10-кратном увеличении
Трансплантацию производили с помощью специального зонда для осеменения. Эмбрионы были помещены в рога матки, через шейку, этот способ назван специалистами цервикальным. Известно, что основным условием хорошего приживления эмбрионов служит синхронность проявления половой охоты у доноров и реципиентов. Следует отметить, что такой синхронности можно добиться в результате тщательного биологического скрининга коров, начиная с начальной стадии подбора и осмотра животных. Как видно, из результатов опыта усовершенствование традиционного биотехнологического метода искусственного осеменения выявило основные достоинства: простоту, экономичность. Способ трансплантации эмбрионов путем прямой пересадки без заморозки от коров-доноров к коровам-реципиентам привел к существенному повышению эффективности получения приплода крупного рогатого скота. Стельность у самок – реципиентов проверялись ректально и с помощью аппарата ультразвуковой диагностики.
Как показали эксперименты, нами проведена трансплантация эмбрионов коровам-реципиентам без заморозки. Традиционно процедура заморозки входила в данный биотехнологический цикл. Результаты выполненных исследований свидетельствуют о том, что усовершенствование традиционного способа искусственного осеменения может обеспечить физиологически нормальную стельность, рождение здоровых телят. Важным условием эффективности эксперимента является четкое исполнение всех фрагментов биотехнологического метода и высокая квалификация специалистов, привлеченных к таким разработкам. В целом, разведение крупного рогатого скота молочных пород с помощью трансплантации эмбрионов позволяет обеспечить размножение высокоценных племенных быков-производителей; формировать поголовье заводских семейств; усилить отбор быков-производителей, повысить генетический статус по селекционным признакам.
Авторы выражают признательность руководителю крестьянского хозяйства Токашеву О.Н., специалистам лабораторией ТОО «БиоПрофи», Асанову Ж.Б., Бекмаганбетову Ж.К., Элистратову Е.В. за помощь и содействие в реализации задач исследования.
Выводы
1. Усовершенствование метода трансплантации эмбрионов без заморозки в сочетании с суперовуляцией у доноров позволяет получить здоровое потомство от высокопродуктивных животных.
2. Процесс трансплантации эмбрионов без заморозки позволяет сокращать срок воспроизведения животных через лучшую его часть поголовья.
3. Применение этого метода позволяет создавать эмбриобанки от генетически ценных животных, сохранять генофонд редких и исчезающих пород.
Библиографическая ссылка
Мухамадиева Н.Н., Кабланов Т.Е., Толымханова З.Н., Советов Ж.Т., Айдарханова Г.С. УСОВЕРШЕНСТВОВАНИЕ МЕТОДА ПРЯМОЙ ПЕРЕСАДКИ ЭМБРИОНОВ ОТ КОРОВ-ДОНОРОВ К КОРОВАМ-РЕЦИПИЕНТАМ // Международный журнал прикладных и фундаментальных исследований. – 2016. – № 7-3. – С. 493-496;URL: https://applied-research.ru/ru/article/view?id=9856 (дата обращения: 27.04.2024).

