Среди всех методов ядерной диагностики только позитронная эмиссионная томография дает возможность визуализации хода биологических процессов in vivo [1], с высоким топометрическим разрешением. Технически это осуществляется помещением в поле зрения ПЭТ-камеры, объекта с введенным радиоактивным изотопом для определения локальной концентрации следовых количеств этого вещества [1, 2].
Цель работы: отработать методику проведения ПЭТ/КТ исследований с мечеными лейкоцитами радиофармпрепаратом «18-фтордезоксиглюкоза» (далее – 18F-FDG) для проведения дифференциальной диагностики воспалительных и злокачественных заболеваний [2–4].
Материалы и методы исследования
В исследовании участвовали здоровые добровольцы после ознакомления с целью исследования и подписания информированного согласия на проведение диагностической процедуры.
ПЭТ/КТ исследование проводили дважды одному и тому же пациенту. Вначале с внутривенным введением 18F-FDG, через 3–5 дней с введением меченных лейкоцитов 18F-FDG.
Синтез радиофармпрепарата 18F-FDG осуществлялся на специализированной производственной линии с контролем качества в каждой партии.
Радиоизотопное исследование проводили на позитронном эмиссионном томографе, совмещенном с компьютерным томографом в режиме «Total body». Из радиофармпрепаратов использовали 18F-фтордезоксиглюкозу (ФДГ), которую вводили медленно внутривенно в дозе 370–420 МБк. Исследование проводится натощак (не меньше 6 часов после приема пищи), с проведением гипергидратации (1,0–1,5 л воды перорально в течение 1 часа после введения радиофармпрепарата) для уменьшения уровня фоновой активности. После инъекции пациент находился в тихом затемненном помещении не менее 60 минут в состоянии покоя, с целью предотвращения накопления ФДГ в активированных мышцах. Перед выполнением исследования пациент опорожнял мочевой пузырь.
Для получения абсолютных значений уровня потребления глюкозы необходимы данные по мгновенному значению распределения активности радиофармпрепарата в тканях, которые исследуются, а также данные по уровню активности препарата в плазме артериальной крови в процессе исследования – «входной функции». Однако при практическом проведении ПЭТ-исследования невозможно получить объективные данные по мгновенному значению концентрации РФП в органах и тканях, поэтому проводится измерение накопленной во время сканирования активности и математически высчитывается среднее значение концентрации. Определение артериальной входной функции обычно осуществляется забором проб крови из катетера, установленного в лучевой артерии в течение всего исследования с наиболее возможной частотой. Эта процедура представляет дополнительные сложности при проведении исследования: во-первых, она является инвазивной и имеет определенные риски развития осложнений, во-вторых, концентрация РФП в крови, полученной из лучевой артерии, отражает не истинную входную функцию (концентрацию препарата в капиллярах ткани) – а относительную и имеет отличия от истинной, во временном сдвиге и в форме, что может являться источником ошибки [1, 2].
В нашем исследовании мы использовали упрощенную оценку метаболизма. Она высчитывалась по формуле: величина метаболизма равна пропорциональной концентрации накопления РФП в интересующей области. Этот полуколичественный метод оценки standartized uptake value (SUV – стандартизированный уровень накопления), является наиболее распространенным и представляет индекс накопления 18F-фтордезоксиглюкозы в тканях, вычисляемый путем нормализации концентрации ФДГ к введенной активности на грамм массы тела [1, 2].
Результаты исследования и их обсуждение
Проведено обследовано 15 здоровых лиц, из них 12 (80 %) женщин и 3 (20 %) мужчин. Возраст пациентов варьировал от 34 до 65 лет. Каждому пациенту присвоен порядковый код исследования. Список пациентов с введенными дозами РФП представлен в табл. 1.
Таблица 1
Список пациентов с введенными дозами РФП
|
№ п/п |
Код |
Дата рождения |
Доза РФП, мКи |
Вес тела, кг |
|
1 |
Код 1 |
03.01.1966 |
10 |
75 |
|
2 |
Код 2 |
14.05.1967 |
14 |
100 |
|
3 |
Код 3 |
19.10.1977 |
9 |
65 |
|
4 |
Код 4 |
14.04.1979 |
8 |
59 |
|
5 |
Код 5 |
29.05.1969 |
13 |
97 |
|
6 |
Код 6 |
14.08.1962 |
12 |
85 |
|
7 |
Код 7 |
13.09.1950 |
10 |
75 |
|
8 |
Код 8 |
29.08.1973 |
7 |
48 |
|
9 |
Код 9 |
25.11.1950 |
5 |
103 |
|
10 |
Код 10 |
18.04.1958 |
10 |
75 |
|
11 |
Код 11 |
20.06.1961 |
12 |
87 |
|
12 |
Код 12 |
08.06.1970 |
11 |
80 |
|
13 |
Код 13 |
10.03.1951 |
7 |
55 |
|
14 |
Код 14 |
21.07.1959 |
9 |
70 |
|
15 |
Код 15 |
30.09.1948 |
10 |
74 |
Одной из задач нашего исследования явилось проведение анализа причинно-следственной зависимости накопления меченных 18F-FDG лейкоцитов в ткани селезенки с эквивалентной дозой радиоактивности [5, 6].
Теоретически мы предполагали накопление меченных 18F-FDG лейкоцитов в селезенке, как показатель активного скопления клеток белой крови в данном органе. Поэтому всем пациентам прицельно измеряли показатель накопления РФП (SUV max) в паренхиме селезенки, как один из достоверных данных о соединении лейкоцитарной массы с радиофармпрепаратом. На основании этого проведен сравнительный анализ количественного соотношения индекса накопления 18F-FDG и меченных лейкоцитов в тканях печени и селезенки у здоровых лиц при ПЭТ/КТ исследовании [5, 6].
Количественное соотношение индекса накопления меченных 18F-FDG лейкоцитов в тканях печени и селезенки у здоровых лиц при ПЭТ/КТ исследовании с 18-фтордезоксиглюкозой и меченных 18F-FDG лейкоцитов представлено в табл. 2.
Таблица 2
Сводная таблица накопления РФП в ткани печени и селезенки
|
Код пациента |
18-фтордезоксиглюкоза |
Меченые лейкоциты 18-фтордезоксиглюкозой |
||
|
в ткани печени |
в ткани селезенки |
в ткани печени |
в ткани селезенки |
|
|
Код 1 |
2,0 |
1,0 |
1,4 |
4,4 |
|
Код 2 |
2,0 |
1,0 |
1,2 |
1,6 |
|
Код 3 |
2,0 |
1,4 |
2,0 |
1,9 |
|
Код 4 |
2,0 |
1,0 |
1,3 |
1,6 |
|
Код 5 |
2,4 |
1,2 |
2,0 |
5,3 |
|
Код 6 |
2,3 |
1,4 |
1,0 |
1,2 |
|
Код 7 |
3,4 |
2,0 |
1,8 |
3,8 |
|
Код 8 |
2,0 |
1,7 |
1,7 |
2,0 |
|
Код 9 |
6,5 |
1,5 |
2,0 |
1,6 |
|
Код 10 |
2,6 |
1,7 |
4,0 |
8,3 |
|
Код 11 |
2,5 |
1,7 |
5,2 |
8,2 |
|
Код 12 |
2,1 |
1,9 |
4,2 |
6,7 |
|
Код 13 |
2,5 |
2,3 |
2,7 |
2,3 |
|
Код 14 |
2,0 |
1,4 |
2,0 |
2,6 |
|
Код 15 |
2,0 |
1,8 |
1,8 |
2,3 |
Как видно из приведенной выше таблицы, отмечается повышение накопления РФП в случае мечения лейкоцитов в паренхиме селезенке в среднем на 57,1 %. На рис. 1 представлены кривые накопления 18F-FDG и 18F-FDG меченных лейкоцитов в паренхиме селезенки.
На рис. 2 представлена диаграмма в сравнительном аспекте индексов накопления 18-FDG и меченных лейкоцитов
18F-DG в паренхиме селезенки.
Анализируя полученные данные, наглядно демонстрируется повышение накопления РФП в случае с меченными лейкоцитами, что подтверждает факт связывания лейкоцитов крови с РФП.
Клинический пример. Код пациента 5. На рис. 3 представлены данные ПЭТ/КТ исследования с измерением SUV max в паренхиме селезенки и печени.
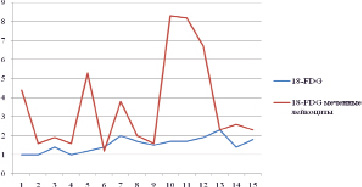
Рис. 1. Кривые накопления (SUV max) в ткани селезенки
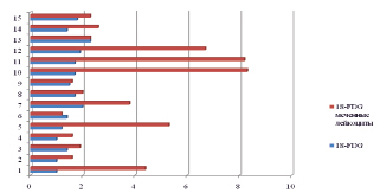
Рис. 2. Гистограмма индексов накопления (SUV max) 18-FDG и меченных лейкоцитов 18-FDG в паренхиме селезенки
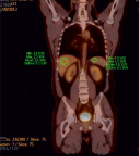
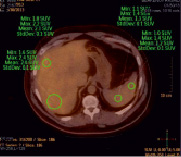
Рис. 3. ПЭТ/КТ-картина (код 5) с введением 18F-FDG
Отмечается визуально повышенное накопление РФП меченных лейкоцитов в паренхиме селезенки. Индексы накопления РФП в паренхиме печени и селезенки представлены на рис. 4, они достоверно свидетельствуют о гиперфиксации РФП в ткани селезенки.
При исследовании с меченными лейкоцитами РФП с одновременным повышением накопления РФП в ткани селезенки отмечается снижение в среднем на 10–12 % накопления РФП в ткани печени. Клинический пример – код пациента 1 на рис. 5, а, б.
На рис. 6 представлена диаграмма в сравнительном аспекте индексов накопления 18-FDG и меченных лейкоцитов
18-FDG в паренхиме печени.
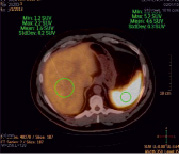
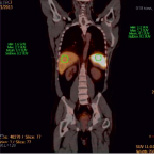
Рис. 4. ПЭТ/КТ-картина всего тела (код 5) с введением 18F-FDG меченных лейкоцитов
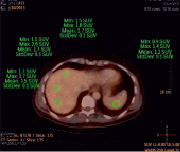
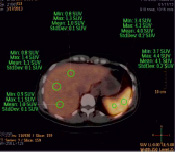
а) б)
Рис. 5. Код пациента 1: а – ПЭТ/КТ-картина с введением 18F-FDG, б – ПЭТ/КТ-картина с введением меченных 18F-FDG лейкоцитов
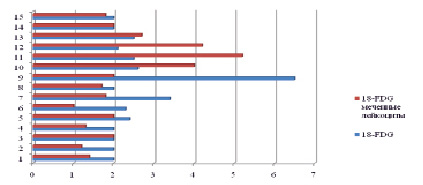
Рис. 6. Гистограмма индексов накопления (SUV max) 18-FDG и меченных лейкоцитов 18-FDG в паренхиме печени
Таким образом, нами установлено повышение накопления меченых лейкоцитов в ткани селезенки с одновременным снижением накопления в паренхиме печени. Полученные путем выделения лейкоцитарной массы из крови больного и соединенные с 18-FDG, лейкоциты связываются с препаратом и устремляются с током крови в ткань селезенки. Данные, полученные в ходе исследования дают надежду на эффективность использования меченных
18-FDG лейкоцитов для дифференциальной диагностики между воспалением и злокачественным поражением.
При анализе исследований нас заинтересовал вопрос о связи накопления 18-FDG и меченных лейкоцитов 18-FDG с дозой введенного РФП. Мы провели корреляционный анализ зависимости накопления РФП в паренхиме селезенки.
Корреляционная зависимость накопления 18-FDG в ткани селезенки с количественным соотношением дозы РФП представлена в табл. 3.
Таблица 3
Корреляционная зависимость накопления 18-FDG в ткани селезенки с дозой введенного РФП
|
Код пациента |
Доза РФП |
Накопление в ткани селезенки (SUV max) |
Коэффициент корреляции |
|
Код 1 |
10 |
1,0 |
– 0,53 |
|
Код 2 |
14 |
1,0 |
–0,62 |
|
Код 3 |
9 |
1,4 |
–0,63 |
|
Код 4 |
8 |
1,0 |
–0,59 |
|
Код 5 |
13 |
1,2 |
–0,54 |
|
Код 6 |
12 |
1,4 |
–0,57 |
|
Код 7 |
10 |
2,0 |
–0,62 |
|
Код 8 |
7 |
1,7 |
–0,52 |
|
Код 9 |
5 |
10,5 |
–0,56 |
|
Код 10 |
10 |
1,7 |
–0,57 |
|
Код 11 |
12 |
1,7 |
–0,56 |
|
Код 12 |
11 |
1,9 |
–0,42 |
|
Код 13 |
7 |
2,3 |
–0,51 |
|
Код 14 |
9 |
1,4 |
–0,50 |
|
Код 15 |
10 |
1,8 |
–0,58 |
Из приведенных данных видно, что отмечена средняя отрицательная корреляция между накоплением РФП в ткани селезенки и введенной дозой радиоактивности препарата, которая свидетельствует о том, что количественное накопление РФП в ткани селезенки достоверно не зависит от дозы введенного препарата.
При определении корреляционной зависимости накопления РФП меченными лейкоцитами в ткани селезенки мы наблюдали обратную картину.
Корреляционная зависимость накопления меченных лейкоцитов РФП в ткани селезенки с дозой введенного РФП представлена в табл. 4.
Таблица 4
Корреляционная зависимость накопления меченных лейкоцитов 18-FDG в ткани селезенки с дозой введенного РФП
|
Код пациента |
Доза РФП |
Накопление в ткани селезенки (SUV max) |
Коэффициент корреляции |
|
Код 1 |
10 |
4,4 |
0,37 |
|
Код 2 |
14 |
1,6 |
0,33 |
|
Код 3 |
9 |
1,9 |
0,38 |
|
Код 4 |
8 |
1,6 |
0,37 |
|
Код 5 |
13 |
5,3 |
0,33 |
|
Код 6 |
12 |
1,2 |
0,39 |
|
Код 7 |
10 |
3,8 |
0,34 |
|
Код 8 |
7 |
2 |
0,38 |
|
Код 9 |
5 |
1,6 |
0,41 |
|
Код 10 |
10 |
8,3 |
0,36 |
|
Код 11 |
12 |
8,2 |
0,37 |
|
Код 12 |
11 |
6,7 |
0,35 |
|
Код 13 |
7 |
2,3 |
0,33 |
|
Код 14 |
9 |
2,6 |
0,33 |
|
Код 15 |
10 |
2,3 |
0,34 |
Как видно из табл. 4, отмечается умеренная положительная корреляционная зависимость между количественным накоплением меченных лейкоцитов РФП в ткани селезенки с введенной дозой препарата.
Вывод – чем больше доза радиофармпрепарата с мечеными лейкоцитами, тем больше накопление препарата в паренхиме селезенки.
Туморотропность испытанных к настоящему времени радиофармацевтических препаратов определяется различными факторами. Часть этих веществ избирательно поступает в опухоль метаболическим путем, в связи с большой утилизацией в опухоли определенных веществ, вследствие изменения ее обмена веществ и более высокой по сравнению с нормальными тканями потребностью в этих продуктах (аминокислоты, некоторые белки, микроэлементы и, др.). Другие препараты могут задерживаться в опухоли механическим путем, вследствие известного изменения опухолевых сосудов, в частности нарушения их проницаемости, наряду с большой васкулярностью некоторых опухолей. Возможно также поступление изотопа в опухоль с использованием меченых антител к известным опухолевым антигенам. Использование известных туморотропных веществ для положительного сканирования в значительной мере повышает диагностическую информацию. Однако отсутствие специфического вещества, тропного только к злокачественным опухолям или воспалительным изменениям, обусловливает определенный процент диагностических ошибок. Ложноположительные результаты бывают значительно реже, чем ложноотрицательные. Это объясняется тем, что туморотропные вещества, как правило, не поступают в доброкачественные опухоли, кисты, рубцовые ткани, но в то же время они не накапливаются в некротизирующихся участках опухоли и, наоборот, способны фиксироваться в активных воспалительных очагах. Последние два момента и таят в себе возможность ошибочных заключений. Данная методика мечения лейкоцитов РФП – 18-FDG дает нам надежду для разработки критериев дифференциальной диагностики между злокачественными и воспалительными заболеваниями, тем самым можно повысить процент истинно положительных заключений при ПЭТ/КТ исследованиях.

