Известно, что активность остеогенеза при лечении различных патологических состояний опорно-двигательного аппарата в значительной степени зависит от кровоснабжения костной и окружающих мягких тканей [4]. В свою очередь создание оптимальных условий для течения репаративных процессов, которые может обеспечить стабильный внеочаговый остеосинтез, благотворно сказывается на состоянии местного кровотока. Одним из решающих факторов в процессах ангиогенеза, артериогенеза и сосудистого ремоделирования является гемодинамика, которая участвует в обеспечении достаточной оксигенации тканей [10]. Состояние сосудов конечностей влияет на морфо-функциональные характеристики кровоснабжаемых мышц [5].
Следовательно, определение особенностей функциональных возможностей сосудов, обеспечивающих регионарное кровоснабжение мягких тканей, имеет ценность в плане прогноза течения и оценки качества проводимого лечения патологических состояний опорно-двигательного аппарата различного генеза.
Целью исследования: явилось изучение особенностей кровообращения в разных группах мышц голени при лечении оскольчатых переломов берцовых костей в условиях чрескостной аппаратной фиксации.
Материалы и методы исследования
Для решения поставленной цели была выбрана экспериментальная модель адекватная клиническим ситуациям. У взрослых беспородных собак (n=18), путем прямого удара, моделировали оскольчатый перелом костей голени типа В3 (классификация АО/АSIF), который через одни сутки после травмы фиксировали при помощи аппарата Илизарова. Сращение перелома происходило через 49,0±1,7 суток аппаратной фиксации.
Выполняли реографию передней большеберцовой и икроножной мышцы оперированного сегмента при помощи реографа-полианализатора РГПА-6/12 «РЕАН-ПОЛИ» (НПКФ «МЕДИКОМ-МТД», Россия) перед моделированием перелома и на следующие сутки непосредственно перед остеосинтезом, через 14 суток фиксации, по окончании периода фиксации и через 30 суток после ее прекращения. Использовали игольчатые электроды. Исследование проводили в утренние часы перед первым кормлением, в помещении с постоянной температурой воздуха 27,7±0,1°С. Всем собакам осуществляли премедикацию общепринятыми фармакологическими веществами.
Анализировали динамику изменений показателей: базисный импеданс (БИ, Ом), время распространения пульсовой волны (ВРПВ, мс), максимальную скорость быстрого кровенаполнения (МСБКН, Ом/с), реографический индекс (РИ, Ом), дикротический индекс (ДКИ, %), диастолический индекс (ДСИ, %). на основании изменений импеданса тканей и величины объемного пульсового кровенаполнения косвенно судили о морфо-функциональном состоянии обследуемой мышцы. В качестве контрольных значений использовали результаты исследований, проводимых до оперативного вмешательства, которые принимали за 100 %.
Выполняли количественную оценку реограмм. Полученные цифровые данные подвергали статистической обработке с использованием компьютерной программы «AtteStat 13.1» (И.П. Гайдышев, Россия). Методами описательной статистики определяли средние величины, стандартное отклонение. Нормальность распределения выборок определяли с помощью критерия Шапиро-Уилка. Результаты исследований обрабатывали методами непараметрической статистики (критерий Вилкоксона для независимых выборок). Различия показателей считали достоверными при р≤0,05.
Эксперименты выполнены в соответствии с требованиями «Европейской конвенции по защите позвоночных животных, используемых для экспериментальных и других научных целей» и были одобрены Комитетом по этике ФГБУ «РНЦ «ВТО» им. акад. Г.А. Илизарова».
Результаты исследования и их обсуждение
При обследовании передней большеберцовой мышцы через 1 сутки после моделирования перелома определяли умеренное повышение тонуса магистральной артерии (a. tibialis anterior), параметр ВРПВ был достоверно ниже контрольных значений на 14,5 % (р=0,05). Артерии крупного, среднего калибра и артериолы находились в состоянии выраженной вазодилятации, МСБКН и ДКИ были ниже контроля на 25,7 % (р=0,05) и более чем на 240 % (р=0,007) соответственно. Венозный отток затруднялся (ДСИ увеличивался на 38,6 %, р=0,047). Уменьшались БИ – на 22,4 % (р=0,06), РИ – на 41 % (р=0,05). Через 14 суток фиксации тонус a. tibialis anterior продолжал повышаться (по отношению к предыдущему периоду обследования на 31,2 %, р=0,07). Вазодилятация артерий крупного и среднего калибра усиливалась, МСБКН понижался еще на 30 % (р=0,06). Вязко-упругие свойства артериол сохранялись на достигнутом уровне. Венозный отток нормализовался. Продолжалось снижение параметров БИ и РИ на 7,6 % и 20 % соответственно (р>0,05). К окончанию периода фиксации (49 суток) функция a. tibialis anterior, сосудов крупного и среднего калибра нормализовалась. В результате объемное кровенаполнение в передней большеберцовой мышце увеличивалось на 75 % (р=0,04) от предыдущего срока обследования, но было ниже физиологической нормы на 15 % (р>0,05). Импеданс повышался на 13 % (р>0,05). В этот период регистрировали наиболее значительные нарушения свойств мелких сосудов, характеризующиеся резко выраженной вазодилятацией (ДКИ снижался еще на 72 %, р<0,05). ДСИ достигал верхней границы нормальных значений, что указывало на тенденцию к формированию нарушения венозного оттока. Через 30 суток после прекращения фиксации эластические свойства магистральной артерии не изменялись. Тонус сосудов крупного и среднего калибра слабо повышался (МСБКН увеличивался на 12 % от контроля, р>0,05). Улучшалась функция артериол (увеличение ДКИ на 32 %, р=0,05). Однако этот параметр был все еще ниже дооперационного уровня. Венозный отток восстанавливался. РИ увеличивался на 7 % (р>0,05), но оставался ниже нормы. БИ достоверно повышался на 17,5 % от контроля. Это свидетельствовало о формировании гисто-структурных изменений обследуемой мышцы, связанных с недостатком ее кровоснабжения на этапе лечения.
На протяжении эксперимента в икроножной мышце изменения гемодинамики были менее выражены в сравнении с передней большеберцовой. Через 1 сутки после моделирования перелома ВРПВ и ДСИ достоверно от контроля не отличались. Снижались параметры: МСБКН (на 25,75 %, р=0,05), ДКИ (более чем на 100 %, р=0,037), БИ (на 14 %, р=0,06) и РИ (на 50 %, р=0,04). Через 14 суток фиксации состояние магистральных артерий не изменялось. Тонус сосудов крупного и среднего калибра повышался, но еще не восстанавливался (МСБКН увеличивался на 12 % от предыдущего срока, р=0,08). ДКИ увеличивался в 4 раза (р=0,021) по отношению к дооперационному уровню, указывая на состояние вазоконстрикции мелких сосудов. Венозный отток был затруднен (ДСИ выше контроля на 38 %, р<0,05). Импеданс не изменялся. РИ увеличивался на 60 % (р=0,021), но оставался ниже дооперационных значений. К окончанию периода фиксации регистрировали тенденцию к повышению тонуса магистральных артерий (ВРПВ достоверно уменьшалось на 10,3 %, (р=0,05) от контроля. Функциональные свойства сосудов крупного и среднего калибра сохранялись на достигнутом уровне и не изменялись до окончания эксперимента. Состояние вазоконстрикции артериол сменялось выраженной вазодилятацией (ДКИ меньше контроля в 9 раз, р=0,001). Это может быть связано с тем, что усиление притока крови в предыдущий период обследования, как следствие резкого повышения тонуса сосудов, являлось механическим раздражителем и привело к структурно-функциональным адаптационным изменениям интимы мелких артерий и артериол, характеризующимся увеличением сосудистого просвета [7, 8]. Венозный отток в этот период нормализовался. Параметры БИ и РИ достигали контрольных значений. Через 30 суток после прекращения фиксации тонус магистральных артерий сохранялся слабо повышенным. Свойства мелких сосудов улучшались, ДКИ увеличивался на 29,5 %, однако дооперационных значений не достигал. Происходило усиление венозного оттока (ДСИ уменьшался в 6 раз, р=0,001). Импеданс увеличивался на 16 %, а объемное пульсовое кровенаполнение снижалось на 15 % от контроля, что косвенно указывало на морфо-функциональное изменение мышечной ткани.
Динамика изменения функциональных свойств сосудов артериального звена и объемного пульсового кровенаполнения отражена на рис. 1-3.
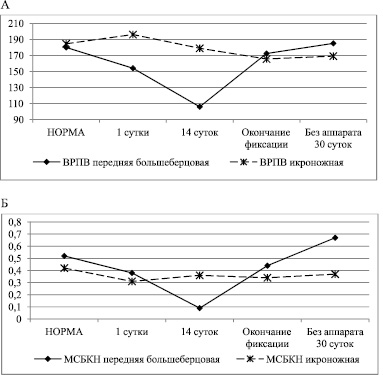
Рис. 1. Динамика изменения функционального состояния: А – магистральных артерий, Б – артерий крупного и среднего калибра передней большеберцовой и икроножной мышцы при лечении переломов костей голени
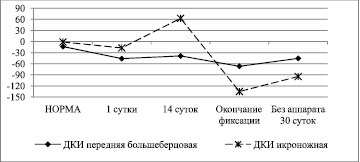
Рис. 2. Динамика изменения функционального состояния сосудов микроциркуляторного русла передней большеберцовой и икроножной мышцы при лечении переломов костей голени
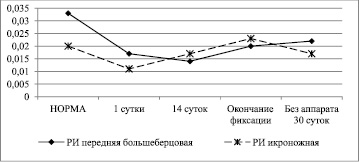
Рис. 3. Динамика изменения объемного пульсового кровенаполнения передней большеберцовой и икроножной мышцы при лечении переломов костей голени
Таким образом, в результате проведенного исследования определили, что через 1 сутки после моделирования перелома костей голени происходило равномерное резкое уменьшение кровенаполнения сосудов мышц сгибателей и разгибателей за счет снижения тонуса артерий крупного, среднего калибра и сосудов микроциркуляторного русла. В этот период в передней большеберцовой мышце происходило затруднение венозного оттока, в икроножной – его нарушение формировалось на раннем этапе фиксации. В последующем венозный отток в мышцах нормализовался. После остеосинтеза кровенаполнение передней большеберцовой мышцы продолжало уменьшаться в результате резкого снижения тонуса сосудов артериального русла, достигая своего минимума через 14 суток фиксации. В дальнейшем функциональные свойства артерий улучшались, что приводило к увеличению притока крови к мышце. Однако его объем через 1 месяц после прекращения фиксации еще не достигал физиологической нормы, как следствие сохранения микроциркуляторных нарушений.
У пациентов при лечении оскольчатых переломов голени методом Илизарова также не отмечали усиленного прироста линейной скорости кровотока по артериям травмированной конечности, что авторы объясняют снижением базального сосудистого тонуса стенок артерий и увеличением их диаметра [6].
В нашем исследовании функциональные свойства сосудов, обеспечивающих кровоснабжение передней большеберцовой мышцы (разгибатель) были более выражены в сравнении с икроножной мышцей (сгибатель). Аналогичные результаты были получены при изучении гемодинамики в разных группах мышц при удлинении голени в области проксимального метафиза [2].
В некоторых работах показано, что в первые 5 суток после накостного остеосинтеза диафизарных переломов костей голени происходил спазм сосудов в проекции надкостницы, который в последующем сменялся гипотонией, преобладающей на всем протяжении последующего периода лечения. В целом процесс регенерации костной ткани протекал в условиях сниженного артериального кровотока и усиленного венозного оттока [3]. В работах других авторов отмечено, что после окончания лечения больных, в частности которым выполняли удлинение голени методом Илизарова, происходила нормализация объемной скорости кровотока, а через 2-6 месяцев после прекращения фиксации наблюдали ее снижение, следовательно, и величины кровенаполнения тканей, в сравнении с исходными значениями [1]. Подобную реакцию регистрировали в выполненном исследовании при оценке кровообращения в икроножной мышце, что также характеризовалось выраженной вазоконстрикцией мелких сосудов в раннем периоде после остеосинтеза, которая сменялась их вазодилятацией в последующем. Восстановление объемного пульсового кровенаполнения мышцы происходило в периоде формирования костного сращения перелома, а после прекращения аппаратной фиксации регистрировали его уменьшение. Этому способствовало сохранение гипотонуса артерий крупного, среднего калибра и артериол, а также усиление венозного оттока вероятно за счет открытия дополнительных сосудистых шунтов.
Без выполнения соответствующих лечебных мероприятий направленных на коррекцию кровообращения, длительное уменьшение притока крови в ранний период после травмы может быть причиной появления апоптоза эндотелиальных и гладкомышечных клеток артерий [9]. Возможно, появление нарушений гемодинамики в мышцах травмированного сегмента в периоде уже после формирования костного сращения связано с возникновением во время лечения изменений деструктивно-репаративного и компенсаторно-приспособительного характера в интиме и внутренней эластической мембране сосудистой стенки.
Заключение
Экспериментально показано, что при оскольчатых переломах берцовых костей (тип В3 по классификации АО/АSIF) в ранний период после травмы происходит резкое уменьшение кровенаполнения мышц голени в результате снижения тонуса сосудов. на этапе лечения изменения функциональных свойств сосудов более выражены в мышцах группы разгибателей, что характеризуется гипокинетическим типом кровотока. В мышцах группы сгибателей в периоде формирования костного сращения объем кровенаполнения восстанавливается, однако в ранний реабилитационный период (после прекращения фиксации) происходит его снижение. Через месяц после прекращения фиксации гемодинамика в мягких тканях голени еще не нормализуется. При лечении переломов костей голени индивидуальный подход к выбору вариантов коррекции кровообращения в разных группах мышц травмированного сегмента, на разных этапах течения репаративного процесса и в периоде реабилитации возможно позволит улучшить окончательный клинический результат лечения пациентов.

