В 10–25 % случаев причиной ишемического инсульта у пациентов в молодом возрасте является спонтанная или травматическая диссекция цервикальных артерий (ДЦА) [1]. По данным крупных популяционных исследований, ДЦА диагностируется в 1,7–2,6, а позвоночных – в 1–1,5 случая на 100 тыс. населения в год. Риск повторного расслаивания сонных артерий в первый месяц составляет около 2 %, в течение года – еще 1 %. Для улучшения комбинированного лечения и функциональных исходов инсультов, связанных с диссекцией, имеет значение своевременно собранный анамнез заболевания, интерпретация неврологического статуса и данные нейровизуализиции [2].
Смертность у пациентов данной группы варьируется в зависимости от локализации диссекции. В экстракраниальных отделах ВСА и ПА составляет приблизительно 5–10 %. Показатели смертности при интакраниальной локализации приближаются к 70 % и выше [3].
Несмотря на усовершенствование методов лучевой диагностики в последние годы, прижизненная диагностика диссекций экстра- инракраниальных артерий по-прежнему остается затруднительной. Весьма специфичным и чувствительным методом диагностики спонтанной и травматической ДЦА является стандартная церебральная ангиография. Широкое распространение получили МР-АГ и КТ-АГ [4, 5, 6, 7]. Классический вид диссекции по данным интраскопии – обнаружение зауженного неравномерного просвета сосуда (интрамуральная гематома). Также характерно наличие пролонгированного стеноза расслоившейся артерии (по типу «крысиного хвоста»), либо полной окклюзии сосуда, с образованием «псевдоаневризмы» или расслаивающей аневризмы. Повторные МР-АГ позволяют выявить характерные для диссекции периоды реканализации. Ультразвуковое исследование фиксирует неспецифические нарушения стенки сосуда и кровотока, как правило требующие дальнейшей верификации [8, 9].
Клиническая значимость спонтанной и травматической ДЦА заключается в развитии транзиторных ишемических атак (ТИА), тяжелого ишемического инсульта или субарахноидального кровоизлияния (САК), требующего специфического эндоваскулярного лечения, в зависимости от состояния сосудистой стенки по данным церебральной ангиографии [10]. Патогенетическим механизмом развития ишемического инсульта при ДЦА является окклюзия, приводящая к «фенестрации интимы», либо формирование ложного просвета сосудистой стенки «псевдоаневризмы», а также инициация процесса тромбогенеза, и, как следствие, эмболия дистальных отделов сосуда, и лишь у незначительного числа больных диагностируется гемодинамический подтип инсульта. Развитие субарахноидальных кровоизлияний возникает вследствие разрыва расслаивающих аневризм [9].
В основе диссекции – слабость артериальной стенки, предположительно вследствие митохондриальной цитопатии. В большинстве случаев диссекция возникает в экстракраниальных сосудах – 88 % (каротидная – 58 %, вертебральная – 30 %). Интракраниальная локализация встречается у 12 % пациентов. Возраст манифестации заболевания в среднем составляет 46,7 лет [11]. В 75 % случаев при ДЦА поражаются проксимальные отделы внутренней сонной артерии (ВСА) (около 2 см дистально к бифуркации), у 15 % пациентов – V1– V2 сегменты позвоночных артерий (ПА). В остальных случаях – дистальные отделы ВСА, СМА, позвоночная артерия (ПА) или основная артерия. Диссекции цервикальных и церебральных артерий могут происходить спонтанно или вторично по отношению к основным или незначительным травмам. У некоторых пациентов они ассоциируются с исходной артериопатией, например, фибромускулярная дисплазия, патологические извитости и изгибы сосудистой стенки, заболевания соединительной ткани, в том числе синдром Марфана, Эрлеса-Данлоса, специфическое и неспецифическое воспаление сосудистой стенки [12, 13].
Типичными симптомами являются головные боли, включая «атипичные лицевые боли», «мигренеподобные» головные боли, имеющие различный характер (тупая, давящая, постоянная, реже пульсирующая или острая); зрительные нарушения, частичный синдром Горнера, пульсирующий шум в ушах, поражение ЧМН и другие очаговые симптомы [14].
Клинический случай. Больная Я., 35 лет, доставлена в ГБ № 17 29.08.2016 г. в 11.07, активных жалоб не предъявляет в связи с речевыми нарушениями, известно, что 9.08.2016 произошло дорожно-транспортное происшествие (ДТП). Из анамнеза известно, что длительное время принимает оральные контрацептивы, курит.
В неврологическом статусе при поступлении – моторная и сенсорная афазия, тонус в правых конечностях снижен, правосторонний гемипарез в руке до плегии, в ноге до 3 баллов, сухожильные и периостальные рефлексы повышены справа, с диссоциацией по оси, патологические знаки справа, правосторонняя гемигипестезия. Координаторные пробы не выполняет в связи с речевыми и двигательными нарушениями. Оценка по шкалам: NIHSS – 12 баллов; Рэнкин – 4; Ривермид – 2; Глазго – 15.
По данным КТ головного мозга от 29.08.2016 в 11.12: патологические изменения вещества головного мозга, травматические повреждения костей свода и основания мозга на момент исследования не выявлены.
Цветовое дуплексное сканирование брахиоцефальных артерий (БЦА) 11.15: признаков гемодинамически значимого стенозирования в артериях правого каротидного бассейна не выявлено; УЗ-признаки диссекции ЛВСА (средняя треть), на расстоянии 32 мм от устья, с явлениями неокклюзирующего тромбоза экстракраниального отдела ЛВСА (по спектральному анализу до 70–75 %). Гемодинамически значимого стенозирования в артериях ВББ не выявлено, вариант «малой» правой позвоночной артерии, кровоток по ПА и ОА компенсирован, D>S, признаков подключично-позвоночного обкрадывания не выявлено. Неравномерность картирования ЛСМА, с акцентом на уровне М1/М2, с локальным увеличением ЛСК до 310 см/с (стенозирование тромбом) ЛСМА до 80 % по спектральному анализу на границе М1/М2).
Осмотр кардиолога от 30.08.2016 г.: Врожденный порок сердца. Недостаточность клапана легочной артерии. Тромбоэмболический синдром? Диагноз: острое нарушение мозгового кровообращения в бассейне левой средней мозговой артерии от 29.08.2016 г. на фоне травматической диссекции слева. Возможно, во время ДТП произошла травматизация внутренней сонной артерии и ее растяжение на поперечных отростках СII–СIII. Принято решение проводить системный троболизис с Актилизе.
Цветовое дуплексное сканирование БЦА после системного тромболизиса: улучшение кровотока по ЛСМА (кровоток картируется на протяжении сегментов М1, М2), скоростные показатели кровотока по ЛСМА на уровне сегмента М1 – в пределах возрастной нормы, на уровне М2 – окальное увеличение ЛСК до 160 см/с (по спектральному анализу) до 60 %. После проведения системного тромболизиса отмечается положительная динамика в неврологическом статусе в виде нарастания силы в правых конечностях в руке до 4 баллов, в ноге – полное восстановление силы до 5 баллов, но речевые нарушения сохраняются, оценка по шкалам NIHSS – 6 баллов; Рэнкин – 4; Ривермид – 2. Пациентке решено провести селективную церебральную ангиографию для определения дальнейшей тактики лечения.
По данным ЦАГ от 29.08.2016 г: определяется протяженная диссекция ЛВСА С5 сегмента (по Е. Fischer); стенозирование тромбом сегмента М1; ретроградное заполнение до уровня М3 через корковые анастомозы и ВББ. С целью профилактики фатального полушарного инсульта пациентке по жизненным показаниям рекомендовано выполнение стентирования левой ВСА (рис. 1а, б, в).
а б в
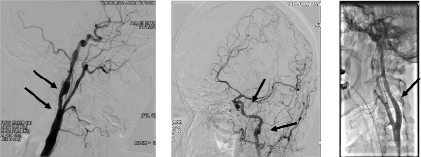
Рис. 1. Селективная церебральная ангиография больной Я., 35 лет, с диагнозом ОНМК по типу ишемии в БЛСМА от 29.08.2016 г. на фоне диссекции ЛВСА: а – определяется протяженная диссекция ЛВСА С5 сегмента (по Е. Fischer); б – стенозирование тромбом сегмента М1; ретроградное заполнение до уровня М3 через корковые анастомозы и ВББ; в – стентирование ЛВСА: в дистальные отделы левой ОСА и в НСА на проводнике заведена проксимальная защита эмболии «Moma» 9F. По проводнику в область протяженной диссекции проведены поочередно, позиционированы и раскрыты 2 стента Precise 7,0х40 мм
В послеоперационном периоде – без нарастания общемозговой и очаговой неврологической симптоматики. На КТ ГМ от 30.08.2016 г. в левой лобной доле определяется гиподенсный очаг с участками геморрагического пропитывания (19х29х30 мм). Рекомендована двойная дезагрегантная терапия в течение 6 месяцев.
Общий генетический риск тромбофилии по исследованным генетическим маркерам находится в пределах общепопуляционных значений.
Оценка когнитивных нарушений в динамике (в острейшем и остром периодах инсульта – 1/8 сутки) по данным нейропсихологического тестирования: амбидекстра; литеральные ассоциации – 0/2 балла; категориальные ассоциации – 0/2 балла; MMSE-5/25 баллов; FAB-7/15 баллов; заучивание и воспроизведение 10 слов – 0/4 балла, тест рисования часов – 0/5 баллов; Бостонский тест называния – 0/6 баллов; тест повторения цифр – 1–1/3–3 баллов; субтест на символьно-цифровое сочетание – 12/18 баллов, тест Бендера – 2/8 баллов. Выраженные когнитивные нарушения смешанного характера в виде дисфункции лобно-подкорковых образований головного мозга слева (быстрая истощаемость когнитивной деятельности, моторная афазия); структур гиппокампового круга (снижение объема зрительной, слухоречевой и оперативной памяти), а также височно-теменно-затылочной области (элементы амнестичекой афазии, конструктивной и динамической апраксии, акалькулии и зрительно-моторной дискоординации). Тест «память» в «Ежедневной жизни: 80/46 баллов. По шкале Гамильтона для оценки депрессии и тревоги: 21/15, что соответствует симптоматической тревоге и депрессии.
В острейшем периоде инсульта у пациентки отмечались выраженные когнитивные нарушения в виде деменции легкой степени выраженности, после проведенной тромболитической терапии и стентирования левой ВСА по жизненным показаниям выявлена тенденция к регрессу когнитивных и двигательных нарушений. 1.09.2016 переведена на отделение неврологии с положительной динамикой в виде частичного регресса моторной афазии и полного восстановления силы в правых конечностях.
Особенностью данного наблюдения является несоответствие временных показателей между травмой и тяжестью последствий (диссекция), что придает травме в этом случае роль не причинного, а провоцирующего фактора в условиях предшествующих диспластических изменений в стенке артерии, позволяя расценивать диссекцию как, возможно, спонтанную [8, 9].
Отдаленные результаты (через три месяца). Очаговая неврологическая симптоматика представлена легкой правосторонней пирамидной недостаточностью. Оценка когнитивных нарушений: литеральные ассоциации – 4 балла; категориальные ассоциации – 4 баллов; MMSE – 28 баллов; FAB – 20 баллов; заучивание и воспроизведение 10 слов – 9 баллов, тест рисования часов – 9 баллов; Бостонский тест называния – 10 баллов; тест повторения цифр – 4–3 баллов; субтест на символьно-цифровое сочетание – 45 баллов; тест Бендера – 16 баллов. Легкие когнитивные нарушения смешанного характера в виде дисфункции лобно-подкорковых образований головного мозга справа: быстрая истощаемость когнитивной деятельности; легкое снижение объема оперативной памяти. Тест «память» в «Ежедневной жизни» – 18 баллов (легкие нарушения памяти), депрессивное расстройство средней степени тяжести и симптоматическая тревога (Шкала Гамильтона 14/15).
По данным МРТ головного мозга определяются кистозно-атрофические изменения в глубоких отделах левой лобной доли, проведена ФМРТ с использованием активирующих заданий (рис. 2а). При выполнении функционального задания определяются участки активации в прецентральной – поле Бродмана 6, постцентральной – Поля Бродмана 2, 3, 1, а также лобной и височной области ПБ 42, 47 слева. Справа активация островкой зоны ПБ13–14 (рис. 2б). При выполнении счетных операций активируются следующие зоны головного мозга: префронтальная и постцентральная кора ПБ 9, 10 с 2-х сторон; верхняя теменная область слева ПБ 7; нижняя теменная область с 2 сторон ПБ 39, 40 – часть зоны Вернике, анализатор сложных профессиональных, трудовых и бытовых навыков. Справа – активация акустико-гностического сенсорного центра речи ПБ 38. Это поле контролирует трудовые процессы, а также ответственно за понимание речи (рис. 2в).
Речевые нагрузки вызывали большое количество активаций в ответ на все предъявляемые стимулы (маркировано оранжевым). Определялись участки активации в латеральных и дорсо-латеральных отделах лобной области ПБ 6, 9, в верхней височной извилине и поясной коре с 2 сторон ПБ32, в задних отделах полушарий мозжечка.
Отличия в организации речевых зон подчеркивают необходимость выявления функциональной асимметрии полушарий головного мозга с использованием прямой стимуляции при выполнении ФМРТ, что может использоваться на этапах коррекции когнитивных нарушений в восстановительном периоде у больных с ишемическим инсультом.
а
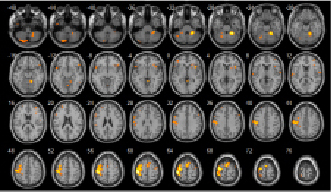
б
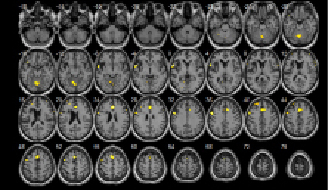
в

Рис. 2. а – ФМРТ больной Я, 35 л., спустя 3 месяца после эндоваскулярного лечения. Тест распознавания предъявляемых изображений, запоминание и фиксация повторяющихся изображений; б – повторяющиеся «простые и сложные счетные операции»; в – исследование автоматизированной и номинативной функции речи «называние простых слов на согласные буквы»
Заключение
Особенностью данного клинического наблюдения является ранняя качественная диагностика и своевременно оказанное комплексное лечение ишемического инсульта на фоне диссекции ЛВСА. Прослежен катамнез сроком 3 месяца, отмечен быстрый регресс очаговой неврологической симптоматики. Проведена оценка когнитивного статуса в динамике с использованием ФМРТ. По данным нейропсихологического тестирования отмечена положительная динамика. При выполнении функциональных заданий выявлено увеличение активаций на все предъявляемые стимулы, а также отличия в организации речевых зон. Определение нейродинамических изменений может являться важной ступенью при лечение когнитивных нарушений у пациентов с ишемическим инсультом.

